Молекулы - это микроскопические частицы, состоящие из атомов, которые связаны между собой химическими связями. Они являются основными строительными блоками всех веществ и имеют свои особенности и свойства.
Основное понятие, связанное с молекулами, - это их химический состав. Каждая молекула состоит из определенного количества атомов, которые могут быть одного или разных элементов. Например, молекула воды состоит из двух атомов водорода (H) и одного атома кислорода (O).
Свойства молекул включают такие химические характеристики, как масса, форма и состояние вещества при определенных условиях. Например, молекулы воды имеют массу 18 г/моль и особенность образовывать связи с другими молекулами воды, что приводит к образованию жидкой формы вещества при комнатных условиях.
Примеры молекул включают молекулы простых веществ, таких как вода (H2O), кислород (O2) и углекислый газ (CO2), а также сложные органические молекулы, такие как ДНК и белки, которые играют важную роль в жизнедеятельности организмов.
Определение молекул

Молекулы состоят из атомов, которые могут быть одинаковыми или разными. Атомы связываются между собой, образуя молекулярные связи. Вещества могут быть молекулярными или атомарными. Молекулярные вещества состоят из молекул, а атомарные вещества состоят из атомов, которые не соединены в молекулы.
Молекулы имеют свойства, которые определяются типом и количество атомов, составляющих молекулу, а также способом связывания атомов. Например, молекулы воды (H2O) состоят из двух атомов водорода и одного атома кислорода, связанных между собой ковалентной связью. Благодаря этой структуре, молекулы воды обладают такими свойствами, как высокая плотность, пониженная кипящая и твердая температура, возможность образования водородных связей и другие химические и физические свойства.
Молекулы являются важными компонентами химических реакций и играют ключевую роль во множестве процессов, происходящих в природе и в живых организмах. Понимание структуры и свойств молекул помогает в изучении химии и других естественных наук, а также находит практическое применение в разных областях, таких как фармацевтика, материаловедение и экология.
Сущность молекул

Молекулы могут быть одноатомными, то есть состоять всего из одного атома, или многоатомными, когда в их составе более одного атома различных элементов. При этом каждый атом в молекуле занимает определенное положение и исполняет определенную роль.
Молекулы обладают такими свойствами, как масса, форма и размеры, которые определяют их физические и химические свойства. Молекулы различных веществ могут иметь разные химические составы и структуры, что определяет их различное поведение в различных условиях.
Примерами молекул могут служить водные молекулы H2O, которые состоят из атомов водорода и кислорода, а также молекулы углекислого газа CO2, состоящие из атома углерода и двух атомов кислорода.
Свойства молекул
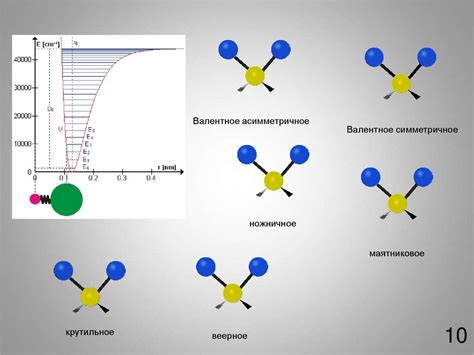
- Масса молекул. Масса молекул определяется суммой масс атомов, составляющих молекулу. Масса может быть разной для разных молекул.
- Геометрическая форма. Молекулы могут иметь различные формы, такие как линейная, плоская или трехмерная.
- Полярность. Молекулы могут быть полярными или неполярными в зависимости от разности электроотрицательностей атомов, входящих в их состав.
- Магнитные свойства. Некоторые молекулы обладают магнитными свойствами и могут образовывать магнитное поле.
- Температурные свойства. Молекулы могут изменять свое состояние при изменении температуры. Они могут находиться в виде газа, жидкости или твердого вещества.
- Химическая активность. Молекулы могут вступать в химические реакции с другими молекулами, образуя новые вещества.
Знание свойств молекул позволяет понять и описать их поведение, а также использовать их в различных практических целях.
Строение молекул
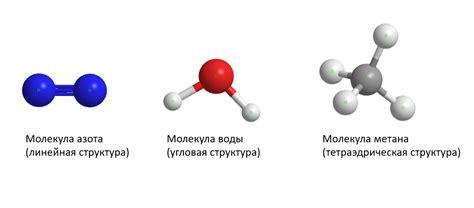
Чтобы представить себе строение молекулы, нужно знать, из каких атомов она состоит и как они связаны друг с другом. Например, вода (H2O) состоит из двух атомов водорода и одного атома кислорода.
Существуют различные типы связей между атомами в молекулах. Одна из самых распространенных связей называется ковалентной связью, при которой атомы обменивают электроны. Есть также ионные связи, где атомы передают электроны друг другу. Кроме того, могут существовать слабые взаимодействия, такие как ван-дер-Ваальсовы силы.
Важно отметить, что строение молекулы может влиять на ее свойства и функции. Например, молекула глюкозы, состоящая из 6 атомов углерода, 12 атомов водорода и 6 атомов кислорода, обладает способностью служить источником энергии для клеток организма.
Изучение строения молекул является основой химии и позволяет лучше понимать множество физических и химических процессов, происходящих в нашей жизни.
Физические свойства молекул

1. Масса молекулы: каждая молекула имеет определенную массу, которая вычисляется путем суммирования масс атомов, из которых она состоит. Масса молекулы определяет ее инерцию и влияет на ее движение.
2. Размер молекулы: молекулы имеют определенные размеры, которые также определяются атомами, из которых они состоят. Размер молекулы влияет на ее взаимодействие с другими молекулами и на ее физические свойства, такие как плотность и вязкость.
3. Форма молекулы: молекулы могут иметь различные формы, такие как линейная, плоская или трехмерная. Форма молекулы также влияет на ее взаимодействие с другими молекулами и на ее химические и физические свойства.
4. Полярность: некоторые молекулы являются полярными, то есть имеют разделение зарядов внутри себя. Это свойство влияет на их способность взаимодействовать с другими полярными и неполярными молекулами и на их растворимость в различных растворителях.
| Физическое свойство | Описание | Пример |
|---|---|---|
| Точка кипения | Температура, при которой жидкость переходит в газовую фазу | Вода - 100°C |
| Точка плавления | Температура, при которой твердое вещество переходит в жидкое состояние | Лед - 0°C |
| Плотность | Масса молекулы, деленная на ее объем | Железо - 7.874 г/см³ |
| Вязкость | Сопротивление молекул движению друг относительно друга | Масло - высокая вязкость |
| Растворимость | Способность молекулы растворяться в определенном растворителе | Соль - растворим в воде |
Эти физические свойства молекул определяют их поведение в различных физических и химических процессах, а также их роль и значение в природе и промышленности.
Химические свойства молекул
Молекулы обладают различными химическими свойствами, которые определяются их составом и структурой. Взаимодействие молекул друг с другом и с окружающими веществами происходит в результате химических реакций.
Одно из важных химических свойств молекул - их способность образовывать соединения. Молекулы могут соединяться между собой, образуя кластеры или полимеры. Некоторые молекулы могут образовывать стабильные соединения с другими веществами при определенных условиях. Например, водород может образовывать соединения с кислородом, образуя воду.
Другое важное химическое свойство молекул - их реакционная способность. Молекулы могут вступать в химические реакции, меняя свою структуру и образуя новые вещества. Например, оксиды могут реагировать с водой, образуя кислоты или основания.
Также молекулы могут обладать окраской. Некоторые молекулы поглощают определенные длины волн света и отражают остальной спектр, что приводит к их окраске. Например, хлорофилловые молекулы в растениях обладают зеленой окраской, так как поглощают большинство излучения красного и синего цветов, а зеленое излучение отражают.
Химические свойства молекул могут быть не только полезными, но и опасными. Например, некоторые молекулы могут быть токсичными или вызывать аллергические реакции у людей. Поэтому важно быть осторожным при работе с химическими веществами и соблюдать необходимые меры предосторожности.
Примеры молекул
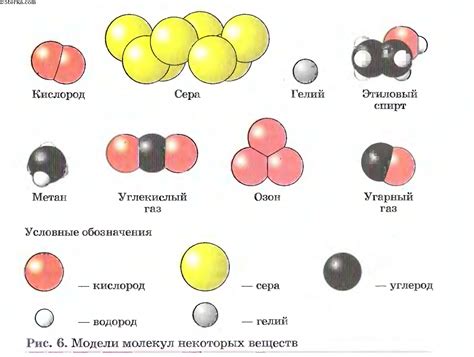
Молекула воды (H2O) состоит из двух атомов водорода и одного атома кислорода. Она является основным компонентом живых организмов и играет важную роль во многих химических реакциях.
Молекула карбоната кальция (CaCO3) состоит из одного атома кальция, одного атома углерода и трех атомов кислорода. Она встречается в виде осадков и является основным компонентом морских раковин и зубов.
Молекула глюкозы (C6H12O6) состоит из шести атомов углерода, двенадцати атомов водорода и шести атомов кислорода. Она является основным источником энергии для организмов и является одним из основных моносахаридов.
Молекула ацетона (C3H6O) состоит из трех атомов углерода, шести атомов водорода и одного атома кислорода. Она широко используется в промышленности и быту в качестве растворителя и очистителя.
Молекула диоксида углерода (CO2) состоит из одного атома углерода и двух атомов кислорода. Она является основным газом, от которого образуются парниковые эффекты и играет важную роль в процессе фотосинтеза.
Это только несколько примеров молекул, которые встречаются в природе и играют важную роль в химических процессах. Молекулы имеют различные свойства и могут образовывать разнообразные соединения в зависимости от их состава и структуры.
Вода

Вода имеет несколько уникальных свойств, таких как высокая теплоемкость, большая теплопроводность, способность мгновенно превратиться в пар и лёд при определенных условиях.
Благодаря этим свойствам вода важна для всех организмов: она участвует в обмене веществ, поддерживает постоянность внутренней среды организма, участвует в химических реакциях и транспорте питательных веществ.
Вода также обладает поверхностным натяжением, благодаря которому жидкость образует сверху пленку, позволяющую насекомым ходить по воде. Это является ещё одной важной особенностью воды.
Вода является универсальным растворителем, способным растворять большинство веществ. Благодаря этому свойству она способствует транспортировке питательных веществ и удалению шлаков из организма.
Примеры веществ, растворимых в воде, включают сахар, соль, кислоты и некоторые газы, такие как кислород и углекислый газ.
Сахар

Белый сахар является самым распространенным видом сахара. Это кристаллическое вещество, состоящее из глюкозы и фруктозы, которые связаны между собой. Сахар обладает сладким вкусом и легко растворяется в воде. Он также может быть использован в качестве консерванта для некоторых продуктов, так как обладает способностью задерживать влагу и предотвращать размножение микроорганизмов.
Сахар является важным источником энергии для организма человека. При употреблении пищи с содержанием сахара, он превращается в глюкозу, которая служит источником энергии для клеток. Однако избыток потребления сахара может привести к проблемам со здоровьем, таким как избыточный вес, кариес, повышенный уровень сахара в крови и др.
Важно отметить, что помимо белого сахара, существуют и другие виды сахара, такие как коричневый сахар, который получается из сырцов с невысокой очисткой и сохраняет большую часть питательных веществ, а также специальные виды сахара, например, фруктоза и сорбитол, которые используются в пищевой промышленности для приготовления диетических и диабетических продуктов.
Кислород

Символично, кислород получил свое название от греческого слова "оксύс", что означает "острый" или "кислый".
Кислород является жизненно важным для многих организмов на Земле, включая растения, животных и микроорганизмы. Он необходим для процесса дыхания и окисления пищи, а также для горения различных веществ. Кроме того, кислород используется в медицине для лечения различных заболеваний и состояний, таких как астма и сердечная недостаточность.
Важно отметить, что кислород является химически активным веществом и образует соединения с различными элементами. Например, с водородом он образует воду (H2O), а с углеродом - углекислый газ (CO2), который также является одним из основных газов атмосферы Земли.