Дистилляция – один из ключевых процессов в химии, позволяющий разделять смеси жидкостей и очищать их от примесей. Это методика, основанная на различной точке кипения компонентов смеси, что позволяет разделить их на составляющие, сконцентрировать или удалить определенные компоненты.
Принцип дистилляции основан на том, что каждое вещество имеет определенную температуру, при которой оно переходит из жидкого в газообразное состояние. При нагревании смеси жидкостей, компоненты с более низкой температурой кипения испаряются в первую очередь и собираются в парообразной фазе. Затем парообразные компоненты охлаждаются и снова становятся жидкостью – этот процесс называется конденсацией. Таким образом, дистилляция позволяет разделить смесь на более легковесные и более тяжелые компоненты.
Применение дистилляции в химической промышленности огромно. Она используется в производстве различных промышленных и бытовых товаров, в процессе получения лекарственных препаратов, в химическом анализе и многих других областях. Например, дистилляция применяется для очистки нефтепродуктов, получения спирта, отделения влаги из растворов, синтеза органических соединений и даже в производстве питьевой воды.
В данной статье мы рассмотрим несколько примеров применения дистилляции в химии, таких как получение эфирных масел из растений, разделение водно-спиртовых смесей, очистка воды в домашних условиях и другие. Мы также рассмотрим различные методы дистилляции, такие как деструктивная дистилляция, вакуумная дистилляция и др.
Определение дистилляции
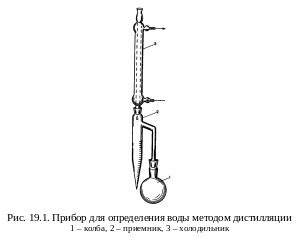
В процессе дистилляции смесь нагревается, чтобы один или несколько компонентов испарились, образуя пары. Пары затем охлаждаются и конденсируются в обратно жидкому состоянию, образуя дистиллят. Компоненты смеси, имеющие более высокие температуры кипения, скапливаются в нижней части дистилляционной колонны, тогда как компоненты с низкими температурами кипения собираются в верхней части.
Кроме того, для многих смесей с близкими температурами кипения может потребоваться использование фракционирования - более сложного процесса разделения смесей. В этом случае дистилляционная колонна оборудуется дополнительными подушками или пластинами, создающими более длительные фракции для отделения компонентов с меньшими различиями в их температурах кипения.
Процесс дистилляции основан на разнице в температурах кипения компонентов смеси и их парообразовании.
Дистилляция широко используется для получения высокочистых продуктов, удаления загрязнений или разделения желательных компонентов. Это важный и эффективный метод разделения смесей, который способствует производству широкого спектра продуктов, необходимых в различных отраслях.
Принципы дистилляции
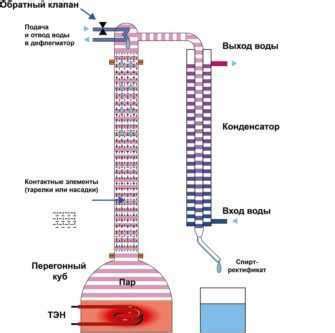
Процесс дистилляции основан на следующих принципах:
- Различие в температуре кипения: Компоненты смеси имеют различные температуры кипения. Во время нагревания, компонент с наименьшей температурой кипения начинает испаряться первым.
- Конденсация паров: Пары компонентов, выходящих из смеси при нагревании, конденсируются при охлаждении. При условии создания определенного давления, конденсация происходит в форме жидкости.
- Сбор и отделение продукта: В результате дистилляции, чистый продукт собирается в отдельную ёмкость, в то время как остаток или неочищенные компоненты остаются в исходной смеси.
Принципы дистилляции применяются в различных областях, включая химическую, нефтяную, фармацевтическую и пищевую промышленность. Этот процесс позволяет получить чистые вещества, удалить примеси и разделить компоненты смеси на полезные фракции.
Важно отметить, что дистилляция требует контроля температуры, давления и других параметров процесса для достижения желаемого результата. Неправильные условия могут привести к неполной очистке смеси или потере ценных компонентов.
Фракционная дистилляция

Процесс фракционной дистилляции широко используется в нефтеперерабатывающей промышленности для разделения нефтепродуктов на различные фракции. К примеру, при дистилляции сырой нефти получаются различные фракции, такие как легкий бензин, керосин, дизельное топливо и т.д. Каждая фракция имеет свой определенный диапазон температур кипения.
Процесс фракционной дистилляции осуществляется в специальной аппаратуре, называемой колонной дистилляции. В колонне дистилляции имеются тарелки или упаковка, которые создают контакт между испаряющимся паром и жидкостью. Благодаря этому контакту происходит разделение компонентов смеси.
На вершине колонны дистилляции находится конденсатор, который охлаждает пары и превращает их обратно в жидкость. После конденсации фракции собираются в отдельные сосуды. Фракции с более высокой температурой кипения конденсируются ближе к низу колонны, а фракции с более низкой температурой кипения - ближе к верху.
Фракционная дистилляция также может быть использована в лабораторных условиях для разделения смесей и получения отдельных компонентов. Например, она может применяться при очистке органических растворителей или при извлечении природных ароматических веществ из растений.
Фракционная дистилляция является важным методом разделения смесей, который находит широкое применение в промышленности и научных исследованиях. Этот процесс позволяет получить высококачественные продукты с нужными физическими и химическими свойствами.
Вакуумная дистилляция

Основное применение вакуумной дистилляции в химии связано с очисткой и разделением сложных смесей веществ. Вакуум позволяет избежать разложения или испарения термолабильных или высококипящих компонентов при повышенной температуре.
Процесс вакуумной дистилляции можно разделить на несколько этапов:
- Напуск вакуума: воздух удаляется из системы, создавая вакуумное пространство.
- Нагрев: смесь поддается нагреву, чтобы она начала испаряться.
- Конденсация: пары из смеси переходят в состояние жидкости в конденсаторе, где они охлаждаются.
- Сбор фракций: полученная жидкость собирается и разделяется на фракции, состоящие из разных компонентов смеси.
Вакуумная дистилляция широко используется в производстве фармацевтических препаратов, нефтепереработке, производстве электроники и других отраслях промышленности, где требуется очистка и разделение сложных смесей веществ.
Помимо промышленности, вакуумную дистилляцию можно использовать и в лабораторных условиях для получения высокочистых веществ или для анализа состава сложных смесей.
Примеры применения дистилляции в химии
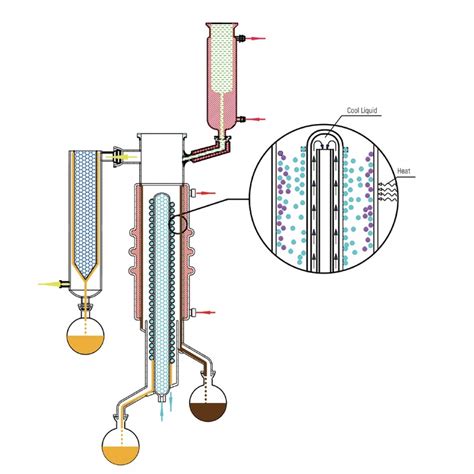
Вот несколько примеров применения дистилляции в химии.
1. Очистка веществ:
Дистилляция обеспечивает эффективное средство очистки различных веществ. Например, при производстве фармацевтических препаратов, дистилляция используется для удаления примесей и влаги из сырого материала, чтобы получить чистые и безопасные лекарственные продукты.
2. Разделение смесей:
Дистилляция позволяет разделить различные компоненты смеси, основываясь на их разных температурах кипения. Это используется, например, для разделения нефти на различные фракции - от легких углеводородов до тяжелых продуктов.
3. Получение растворов:
Дистилляция может также применяться для получения растворов с заданной концентрацией. Например, с помощью дистилляции можно получить водный раствор с определенным содержанием соли или другого вещества.
4. Подготовка реактивов:
В лаборатории дистилляция используется для приготовления высокочистых реактивов, которые требуются для проведения химических реакций. Это позволяет избежать примесей и улучшить качество реагентов.
5. Переработка спиртных напитков:
Дистилляция широко применяется в процессе производства спиртных напитков, таких как водка, виски и сикел. Она используется для разделения этилового спирта от других компонентов смеси, таких как вода и ароматические соединения.
Все эти примеры показывают важность дистилляции в химической промышленности и научных исследованиях. Она является незаменимым инструментом в процессе разделения и очистки смесей, позволяя получать чистые вещества и оптимизировать производственные процессы.
Ограничения и проблемы дистилляции

Несмотря на свою эффективность, дистилляция в химии имеет свои ограничения и может сталкиваться с определенными проблемами. Решение этих проблем требует дополнительных мер и техник для обеспечения успешного процесса дистилляции.
Одно из основных ограничений дистилляции заключается в ее применимости только к веществам, которые могут быть легко испарены и имеют различные температуры кипения. Вещества с высокими температурами кипения и более сложные смеси, содержащие ряд компонентов с близкими температурами кипения, могут представлять сложности для процесса дистилляции.
Еще одной проблемой является возможность разрушения или изменения химического состава исходного вещества во время дистилляции. Высокие температуры и другие факторы, связанные с процессом, могут привести к разложению или реакции вещества, что может повлиять на его конечное качество.
Подбор правильного типа и размера оборудования также является важным аспектом дистилляции. Неправильная конструкция или выбор оборудования может привести к низкой эффективности процесса или даже опасностям, связанным с неправильной работой оборудования.
Другой проблемой, с которой может столкнуться дистилляция, является выбор правильного типа и размера уплотнительного материала. Некоторые вещества могут иметь специфические требования к уплотнителям, и неправильный выбор может привести к утечке или контаминации исходного вещества.
Также важно учитывать, что дистилляция может быть энергоемким процессом, особенно при использовании высоких температур. Поэтому снижение энергозатрат может быть одной из задач, которую нужно решать при проведении дистилляции.
Несмотря на эти ограничения и проблемы, дистилляция остается одним из основных методов разделения и очистки в химии. Благодаря правильному подходу и соответствующему оборудованию, можно достичь высокой эффективности и получить чистые продукты.