Ионная связь – один из видов химической связи между атомами или ионами. Этот тип связи возникает между атомами, когда один из них переходит в ионное состояние и образует ион положительного или отрицательного заряда.
Ионная связь является результатом электростатического притяжения между положительно и отрицательно заряженными ионами. Она встречается в множестве неорганических соединений, таких как соли и металлы, а также в некоторых органических соединениях.
Ионная связь – очень сильная связь, так как требуется большая энергия для разрушения электростатического притяжения между ионами. Поэтому вещества, содержащие ионные связи, как правило, обладают высокой температурой плавления и кипения.
Атомы ионов
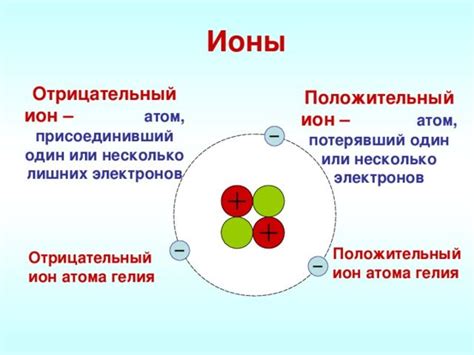
Атомы могут стать ионами путем потери или приобретения электронов. Когда атом теряет электрон(ы), он становится положительно заряженным ионом, называемым катионом. Когда атом приобретает электроны, он становится отрицательно заряженным ионом, называемым анионом.
Катионы и анионы имеют разные размеры и химические свойства из-за разных количеств электронов в их валентной оболочке. Например, катионы обычно имеют меньший радиус, чем их соответствующие нейтральные атомы, потому что потеря электрона приводит к сокращению электронных оболочек.
Ионы в ионной связи притягиваются друг к другу и образуют кристаллическую решетку, в которой положительные ионы окружены отрицательными ионами и наоборот. Это образует прочную структуру, которая обладает высокой твердостью и точкой плавления.
| Тип иона | Заряд иона | Примеры |
|---|---|---|
| Катион | Положительный (+) | Na+ (натрий), Mg2+ (магний) |
| Анион | Отрицательный (-) | Cl- (хлор), O2- (кислород) |
Ионная связь имеет широкое применение как в неорганической, так и в органической химии. Она играет важную роль в образовании солей, минералов, кислот и щелочей, а также в процессах растворения и кристаллизации веществ.
Электроны и ионные связи
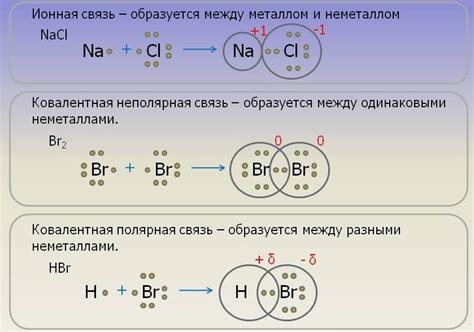
В ионной связи один атом становится ионом с положительным зарядом (катионом), а другой атом становится ионом с отрицательным зарядом (анионом). Заряды разнополярных ионов притягиваются друг к другу, образуя прочную химическую связь.
Электроны играют ключевую роль в формировании ионных связей. Когда один атом отдает электроны, они переходят к атому, который принимает электроны, образуя пару ионов с разными зарядами. Это взаимодействие происходит под воздействием электростатической силы притяжения между различно заряженными ионами.
Ионные связи обычно возникают между металлами и неметаллами. Металлы способны отдать электроны, образуя катионы, которые имеют положительный заряд. В свою очередь, неметаллы могут принимать электроны, образуя анионы, имеющие отрицательный заряд. Такое перераспределение электронов позволяет образовывать ионные соедине
Создание ионов

Ионы образуются путем перехода электронов между атомами, что происходит в химических реакциях. Образование ионов связано с изменением электрического заряда атомов или молекул.
В реакциях образования ионов два типа процессов играют ключевую роль: ионизация и диссоциация.
Ионизация - это процесс, при котором атом или молекула приобретает или теряет один или несколько электронов, превращаясь в ион. Аtom или молекула, которая теряет электрон, называется катионом, имеющая положительный заряд, в то время как атом или молекула, которая приобретает электрон, называется анионом, имеющая отрицательный заряд.
Диссоциация - это процесс, при котором ионная соединение распадается на ионы в растворе. В этом случае ионы образуются из атомов, которые ранее были связаны химической связью, но теперь разделены в растворе.
Образование ионов является важной составляющей процессов, происходящих во многих аспектах химии, таких как электролитическая диссоциация, реакции окисления-восстановления, кислотно-щелочные реакции и многое другое.
Свойства ионов
Электрический заряд: каждый ион имеет определенный положительный или отрицательный электрический заряд. Положительные ионы называются катионами, а отрицательные - анионами. Электрический заряд определяет взаимодействие ионов с другими веществами и их участие в реакциях.
Растворимость: различные ионы могут иметь разную степень растворимости в разных средах. Некоторые ионы легко растворяются в воде, образуя электролитические растворы, в то время как другие могут быть менее растворимыми или вообще нерастворимыми.
Химическая реактивность: ионы обладают высокой химической реактивностью, так как их электрический заряд может влиять на их способность взаимодействовать с другими веществами. Катионы и анионы могут образовывать новые соединения с различными элементами и молекулами.
Поляризуемость: поляризуемость ионов определяет их способность создавать электрические поля вокруг себя. Ионы с большим электрическим зарядом и малым размером могут быть сильно поляризованными, что влияет на их взаимодействие с другими ионами и молекулами.
Валентность: ионы могут иметь различную валентность, что означает различное количество потерянных или приобретенных электронов. Валентность определяет способность ионов образовывать связи с другими элементами и молекулами, а также их степень стабильности.
Все эти свойства ионов играют важную роль в понимании химической реактивности и веществ, в которых присутствуют ионы. Они также влияют на формирование солей, кислот и оснований, а также на растворимость различных соединений.
Влияние ионной связи на свойства вещества
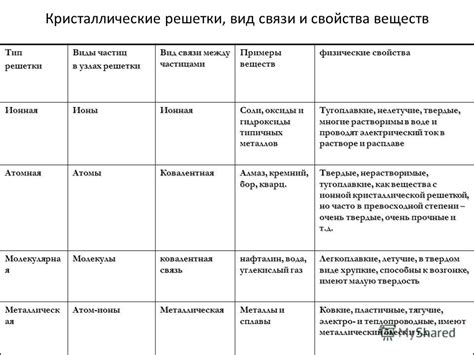
| Свойство вещества | Влияние ионной связи |
| Точка плавления и кипения | Ионные соединения обычно имеют высокие температуры плавления и кипения, так как для разрыва ионной связи требуется большое количество энергии. |
| Растворимость | Ионные соединения часто хорошо растворяются в воде, так как положительные и отрицательные ионы разделяются и притягиваются к полярным молекулам воды. |
| Проводимость | Ионные соединения обладают хорошей электропроводностью в расплавленном состоянии или в растворе, так как ионы могут свободно двигаться и несут электрический заряд. |
| Твердотельные структуры | Ионные соединения образуют кристаллические структуры, где положительные и отрицательные ионы располагаются в определенном порядке. |
| Химическая реактивность | Ионные соединения часто участвуют в реакциях, связанных с обменом ионами или образованием новых ионных соединений. |
Таким образом, ионная связь играет ключевую роль в определении различных свойств вещества. Понимание этого влияния помогает объяснить множество химических явлений и реакций, а также находит применение в различных областях науки и технологий.
Ролевая игра ионов в химических реакциях

Ионы играют важную роль в химических реакциях, так как именно они обладают электрическим зарядом и способны образовывать ионные связи.
Ионная связь основана на притяжении между ионами с противоположными электрическими зарядами. Катионы, имеющие положительный заряд, притягивают анионы с отрицательным зарядом. Таким образом, образуются структуры, в которых ионы расположены регулярно в кристаллической решетке.
Ионы могут участвовать в химических реакциях в качестве реагентов, продуктов или катализаторов. При реакции ионные связи могут разрушаться или образовываться, что приводит к образованию новых веществ.
Процессы, связанные с ионами, происходят как в растворах, так и в твердых веществах. В растворах ионы свободно перемещаются и могут взаимодействовать с другими ионами или молекулами. В твердых веществах ионы образуют кристаллические решетки, которые обеспечивают прочность материалов.
Ионные реакции имеют большое значение в различных областях науки и технологии. Например, они играют важную роль в электролизе, где происходит разложение вещества под воздействием электрического тока. Ионы также используются в батареях, где происходит трансформация химической энергии в электрическую.
Разновидности ионной связи
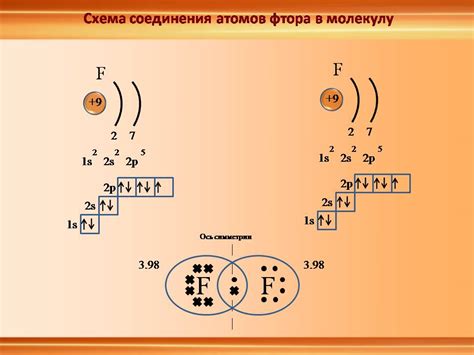
В химии существует несколько разновидностей ионной связи, которые варьируются в зависимости от типа ионов и их взаимодействия.
1. Простая ионная связь: это наиболее распространенная форма ионной связи, где положительно заряженный ион и отрицательно заряженный ион просто притягиваются друг к другу. Пример такой связи - натрий (Na+) и хлор (Cl-) в хлориде натрия (NaCl).
2. Координационная ионная связь: в этом случае положительно заряженный ион притягивается к отрицательно заряженным атомам, которые составляют комплексную молекулу. Пример такой связи - комплексные соединения переходных металлов, например, гексаамминникель(II) хлорид - [Ni(NH3)6]Cl2.
3. Ион-дипольная связь: это взаимодействие между ионом и заряженным диполем, таким как молекула воды. Вода - это ион-дипольное соединение, где заряженные ионы притягиваются к частично заряженным концам молекулы H2O.
4. Ион-ионная связь в решетке кристаллов: это связь, образованная между положительно и отрицательно заряженными ионами в кристаллической решетке. Примером такой связи является кристаллическая структура соли - NaCl.
Ионная связь играет важную роль в химии, обеспечивая стабильность и структуру различных компонентов веществ и соединений. Понимание разных разновидностей ионной связи поможет нам более глубоко изучать химические реакции и свойства различных материалов.
Применение ионной связи

Ионная связь имеет широкое применение в химии и других областях науки и технологий. Вот несколько примеров использования этого типа связи:
1. Соли
Ионная связь играет ключевую роль в формировании солей. Соли образуются при взаимодействии положительно и отрицательно заряженных ионов. Это включает в себя соединения металлов с неметаллами, такие как хлорид натрия (NaCl) и сульфат кальция (CaSO4).
2. Обработка воды
Ионная связь используется для обработки воды. Например, процесс обратного осмоса включает использование наличия ионов соли в оригинальной воде для отделения и удаления органических и неорганических веществ, чтобы получить чистую питьевую воду.
3. Электролиты
Электролиты, такие как соли и кислоты, являются важными компонентами во многих химических процессах и электрохимических устройствах. Они создаются путем диссоциации ионов в растворе и обеспечивают проводимость электрического тока.
4. Лекарства и биологические процессы
Многие лекарственные препараты содержат ионы, которые взаимодействуют с биологическими молекулами в организме человека, такими как белки. Эти взаимодействия могут изменять функции белков и воздействовать на биологические процессы внутри организма.
5. Поверхностно-активные вещества
Ионные связи также играют важную роль в поверхностно-активных веществах, таких как моющие средства и различные пены. Эти вещества содержат гидрофильные и гидрофобные группы ионов, которые позволяют им эффективно взаимодействовать с водой и другими поверхностями.
Это лишь несколько примеров применения ионной связи в химии и других областях. Этот тип связи играет важную роль в множестве процессов и технологий, которые мы используем ежедневно.