Растворимость пептидов в воде является одним из ключевых исследовательских вопросов в области биофизики и фармакологии. Пептиды, состоящие из аминокислотных остатков, могут проявлять различную степень растворимости в воде в зависимости от ряда факторов.
Один из факторов, определяющих растворимость пептидов, - это их аминокислотный состав. Некоторые аминокислоты обладают гидрофильными свойствами и способствуют увеличению растворимости пептида, в то время как другие аминокислоты могут быть гидрофобными и снижать растворимость. Таким образом, состав аминокислот в пептиде может влиять на его взаимодействие с водой и его растворимость.
Еще одним фактором, влияющим на растворимость пептидов, является длина пептидной цепи. Короткие пептиды обычно имеют повышенную растворимость в воде, поскольку их молекулы могут легко перемещаться и образовывать связи с молекулами воды. Для более длинных пептидов может возникнуть проблема агрегации, когда молекулы пептида начинают взаимодействовать друг с другом, что может снижать растворимость в воде.
Другим фактором, который может влиять на растворимость пептидов в воде, является растворитель. Некоторые пептиды могут быть растворимы в одних растворителях, но нерастворимы в других. Наличие определенных ионов или органических растворителей может сильно повлиять на растворимость пептида.
Все эти факторы сложно учесть при разработке новых пептидных препаратов или при проведении исследований по биофизике. Однако, понимание этих факторов позволяет ученым прогнозировать растворимость пептидов и выбирать оптимальные условия эксперимента или применения пептида в медицине.
Факторы, способствующие растворимости пептидов в воде

1. Длина и аминокислотный состав пептида: Длина пептида и аминокислотный состав имеют значительное влияние на его растворимость в воде. Обычно, короткие пептиды лучше растворяются в воде, чем более длинные. Кроме того, определенные типы аминокислот могут способствовать растворимости пептида в воде, такие как поларные аминокислоты (например, глутамин, аспарагин) или аминокислоты с заряженными группами (например, лизин, аргинин).
2. Заряд пептида: Заряд пептида может существенно влиять на его растворимость в воде. Пептиды с зарядами, соответствующими pH среды, часто более растворимы, чем пептиды с обратными зарядами. Кроме того, наличие заряженных групп в пептидах может способствовать образованию ионных связей с водой, что также улучшает их растворимость в воде.
3. Гидрофобность: Гидрофобные взаимодействия между аминокислотами пептида могут приводить к его низкой растворимости в воде. Однако, присутствие поларных групп или групп с зарядами может частично компенсировать гидрофобное взаимодействие и повысить растворимость пептида в воде.
4. Вторичная структура: Вторичная структура пептида, такая как альфа-спирали или бета-складки, может ограничивать доступ воды к гидрофильным регионам пептида, что снижает его растворимость в воде. Напротив, разворотные структуры, такие как случайные катушки или нежесткие структуры, могут способствовать растворимости пептида в воде.
5. Температура: Температура является фактором, который может оказывать значительное влияние на растворимость пептида в воде. При повышении температуры растворимость пептида в общем случае увеличивается, так как повышение температуры способствует разрушению гидрофобных взаимодействий и увеличению движения молекул воды.
Однако, необходимо отметить, что растворимость пептидов в воде - сложная характеристика, которая зависит от многих факторов, и ее предсказание может быть нетривиальной задачей. В этом контексте, дальнейшие исследования и эксперименты могут помочь лучше разобраться в этой проблеме и оптимизировать растворимость пептидов для различных приложений.
Химический состав пептидов
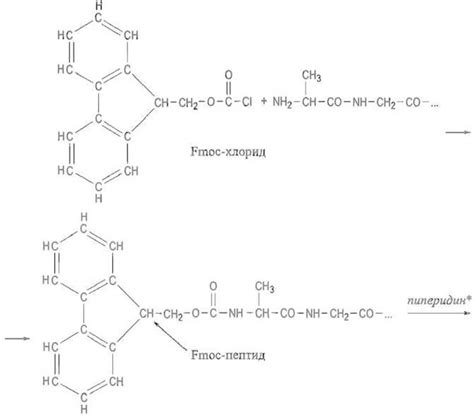
Аминокислоты, входящие в состав пептидов, представляют собой органические соединения, содержащие аминогруппу (-NH2), карбоксильную группу (-COOH) и боковую цепь, которая определяет свойства каждой конкретной аминокислоты. Существует 20 стандартных аминокислот, которые могут входить в состав пептидов и белков.
В молекуле пептида различные аминокислотные остатки связаны между собой пептидными связями, образующими цепочку. Пептидные связи образуются при взаимодействии карбоксильной группы одной аминокислоты с аминогруппой другой аминокислоты. Молекулы воды отщепляются при образовании пептидной связи, что приводит к образованию полипептидной цепи.
Таким образом, химический состав пептидов включает в себя аминокислотные остатки, связанные пептидными связями, и определяет их структуру и свойства. Различный состав аминокислот в пептиде может влиять на его растворимость в воде, стабильность и функциональные свойства.
Размер пептидной цепи
Размер пептидной цепи играет важную роль в растворимости пептидов в воде.
Краткосрочные пептиды обычно имеют меньшую тенденцию к растворению в воде, поскольку их маленький размер не обеспечивает достаточное количество групп, способных взаимодействовать с водой. Это может быть связано с ограниченным количеством полюсных групп или возможных связей водородной связи.
Пептиды с более длинной цепью, наоборот, обычно более растворимы в воде. Большой размер пептидной цепи позволяет образовываться большему количеству связей водородной связи и более эффективно взаимодействовать с молекулами воды. Это повышает растворимость пептида и способствует его диссоциации в водной среде.
Однако с увеличением размера пептидной цепи возрастает вероятность образования внутримолекулярных взаимодействий, таких как гидрофобные взаимодействия, которые могут снизить растворимость пептида. Использование дополнительных групп, таких как заряженные аминокислоты, может помочь увеличить растворимость пептида большого размера.
Таким образом, размер пептидной цепи является важным фактором, определяющим его растворимость в воде. Оптимальное соотношение размера и состава аминокислот может быть определено для каждого конкретного пептида с учетом его конечного использования и внутримолекулярных взаимодействий.
Аминокислотный состав пептидов

Часто пептиды, содержащие большое количество положительно заряженных аминокислотных остатков, таких как аргинин или лизин, имеют повышенную растворимость в воде. Это объясняется тем, что положительные заряды на аминокислотных остатках могут образовывать электростатические взаимодействия с отрицательно заряженными молекулами воды.
С другой стороны, пептиды с большим количеством аминокислотных остатков, имеющих отрицательный заряд, таких как аспартат или глутамат, могут иметь низкую растворимость в воде. В таких случаях, отрицательные заряды аминокислотных остатков могут конкурировать с отрицательно заряженными молекулами воды, что уменьшает взаимодействие между пептидом и растворителем.
Также стоит отметить, что химические свойства аминокислотных остатков, такие как гидрофильность или гидрофобность, также могут влиять на растворимость пептидов в воде. Гидрофильные аминокислотные остатки могут образовывать водородные связи с молекулами воды и, следовательно, повышать растворимость пептида. В то же время, гидрофобные аминокислотные остатки могут предпочитать взаимодействовать сами с собой, образуя гидрофобные ядра внутри пептида и, таким образом, уменьшая его растворимость в воде.
Физико-химические свойства пептидов
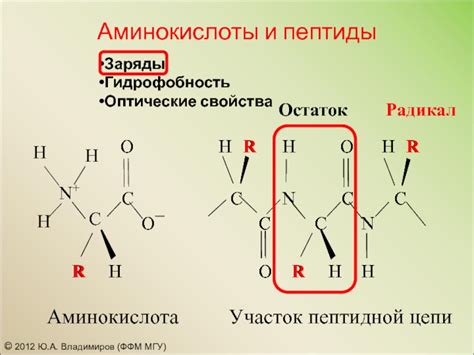
- Аминокислотный состав: определенный набор аминокислот в составе пептидов подразумевает наличие конкретных функциональных групп, которые определяют их способность к образованию водородных связей, ван-дер-Ваальсовых взаимодействий и других сил притяжения.
- Размер и геометрия молекулы: геометрическая форма пептидов может влиять на их способность образовывать структуры вторичной и третичной структуры (α-спираль, β-лист и т. д.) и взаимодействовать с другими молекулами.
- Заряд пептидов: пептиды могут быть заряженными (катионами или анионами) или зарядовые нейтральными. Зарядность пептидов может влиять на их способность образовывать ионообменные связи и взаимодействовать с растворителем.
- Гидрофобность: состав аминокислот в пептидном цепочке может определять его гидрофобный или гидрофильный характер. Гидрофобные пептиды обычно менее растворимы в воде, в то время как гидрофильные пептиды легко растворяются.
- Температура и pH: физико-химические свойства пептидов могут меняться в зависимости от температуры и pH раствора. Изменение этих параме-тров может вызывать структурные изменения и определенные свойства пептидов.
Все эти факторы взаимодействуют и влияют на растворимость и другие физико-химические свойства пептидов, делая их сложными объектами изучения и применения в различных областях науки и медицины.
Интеракции с молекулами воды
Когда пептид попадает в воду, молекулы воды охватывают пептид и взаимодействуют с его атомами и группами. Взаимодействие между молекулами воды и пептидом обеспечивает стабильность структуры пептида и его растворимость в воде.
Одной из основных форм взаимодействия между молекулами воды и пептида является водородная связь. Водородная связь образуется между положительным атомом водорода и отрицательно заряженным атомом кислорода или азота пептида. Это взаимодействие способствует стабилизации структуры пептида в водной среде.
Кроме того, молекулы воды могут с помощью водородных связей образовывать сеть вокруг пептида, что создает гидратационную оболочку вокруг пептида. Гидратационная оболочка предотвращает взаимодействие пептида с другими молекулами, такими как белки или липиды, и улучшает его растворимость в воде.
Влияние окружающей среды на растворимость пептидов
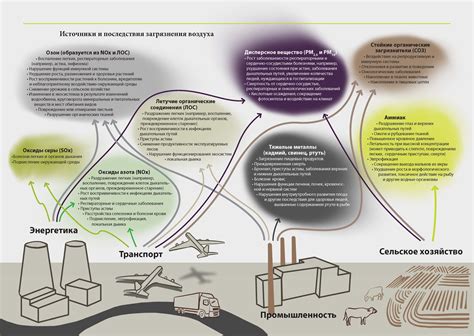
Окружающая среда играет важную роль в растворимости пептидов в воде. Различные факторы окружающей среды могут оказывать влияние на структуру и взаимодействие пептидов, что в конечном итоге влияет на их растворимость.
Один из ключевых факторов, влияющих на растворимость пептидов, - это рН окружающей среды. Растворимость пептидов обычно зависит от их изоэлектрической точки, которая является рН значения, при котором электрический заряд пептида равен нулю. В зависимости от рН окружающей среды, пептид может иметь положительный или отрицательный заряд, что влияет на его способность растворяться в воде. Это объясняется электростатическими взаимодействиями между заряженными аминокислотными остатками пептида и молекулами воды.
Температура также играет важную роль в растворимости пептидов. При повышении температуры, энергия молекул воды увеличивается, что приводит к увеличению движения и взаимодействия молекул пептида с водой. Это может способствовать большей растворимости пептида в воде. Однако высокие температуры могут также вызывать денатурацию пептидов, что влечет за собой потерю их растворимости.
Соли и другие добавки могут также влиять на растворимость пептидов в воде. Наличие ионов в окружающей среде может изменять электростатические взаимодействия пептида со своим окружением и влиять на его растворимость. Некоторые ионы могут стабилизировать структуру пептида и способствовать его растворимости, в то время как другие могут вызывать его агрегацию и снижение растворимости.