Углерод – элемент, обладающий большим разнообразием свойств и являющийся одним из фундаментальных компонентов органической химии. Несмотря на свою превалирующую металлическую природу, углерод выделяется своими высокими неметаллическими свойствами, которые позволяют ему образовывать огромное количество различных соединений и структур.
Одним из наиболее известных и распространенных проявлений неметаллических свойств углерода является его способность образовывать ковалентные связи с другими элементами. Это позволяет углероду образовывать различные органические соединения, такие как углеводороды, аминокислоты и жирные кислоты. Ковалентные связи между атомами углерода обуславливают его способность образования различных структур, включая простые линейные цепи, кольцевые структуры и сложные трехмерные конструкции.
Благодаря неметаллическим свойствам углерода, он играет ключевую роль в множестве процессов и явлений в живой природе. Углерод является основным строительным элементом органических молекул, таких как ДНК, РНК и белки. Благодаря способности образовывать большое количество различных соединений, углерод является основой для создания изделий из пластика, композитных материалов и активного угля, который широко используется для очистки и фильтрации воды и воздуха.
Таким образом, неметаллические свойства углерода не только обеспечивают его высокую выраженность в органической химии, но и позволяют использовать его в различных областях жизни, начиная от медицины и энергетики и заканчивая промышленностью и экологией.
Углерод: особенности химического элемента
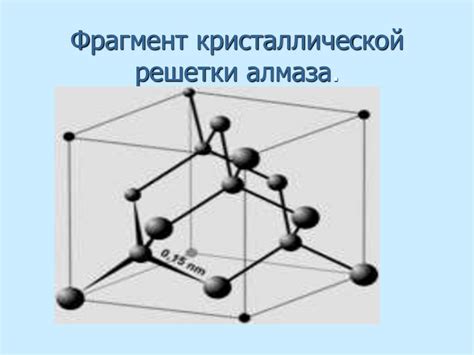
Символ углерода – С. Он относится к группе четырех атомов, известных как группа 14, и находится в четвертом периоде.
Одним из наиболее известных и распространенных форм углерода является алмаз. Алмазы впечатляют своей твердостью и блеском, их используют в ювелирном и промышленном производстве. Другая форма углерода – графит, который используется в карандашах благодаря своим мягким и смазывающим свойствам.
Кроме того, углерод встречается и в других формах: аморфном углероде, углеродных нанотрубках, фуллеренах и графене. Они имеют свои специфические свойства и широко применяются в различных областях науки и техники.
Углерод является неотъемлемой частью органической химии, так как является базисом для всех органических соединений. Большинство органических соединений содержат углерод и формируют основу биологических молекул, включая углеводы, липиды, белки и нуклеиновые кислоты.
Благодаря своей уникальной способности образовывать связи с другими атомами углерод играет роль строительного блока жизни и является одним из самых важных элементов в химии.
Легендарная неметаллическая реактивность углерода
Одной из самых известных реакций углерода является его взаимодействие с кислородом. Под действием высоких температур углерод может сгорать, образуя углекислый газ. Эта реакция известна как окисление углерода и играет важную роль в процессе горения органических веществ. Кроме того, углерод может образовывать оксиды, такие как углекислый газ и оксид углерода, которые важны для многих процессов в природе и промышленности.
Углерод также проявляет свою реактивность во взаимодействии с другими элементами, такими как водород, азот, фосфор и сера. В результате этих реакций образуются многочисленные соединения, такие как метан, этилен, диоксин и многие другие. Многие из этих соединений имеют важное значение для жизни на Земле, так как являются основными компонентами органического вещества.
Как неметалл, углерод обладает способностью образовывать ковалентные связи с другими атомами углерода, что приводит к образованию разнообразных форм и структур, включая алмазы и графит. Алмаз – один из самых твердых известных материалов, а графит – один из самых мягких. Это обусловлено различными структурами, в которых атомы углерода соединены друг с другом.
В целом, углерод является уникальным неметаллом, обладающим легендарной реактивностью и способностью образовывать разнообразные соединения и структуры. Его свойства и химические реакции имеют решающее значение для многих аспектов нашей жизни, начиная от процессов горения и заканчивая созданием новых материалов и технологий.
Углеродные аллотропы: нескончаемое разнообразие
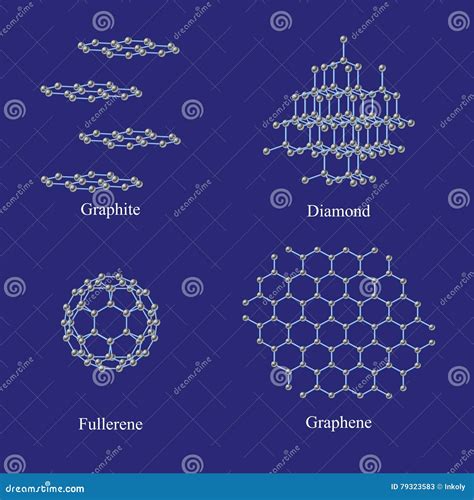
Наиболее известными углеродными аллотропами являются алмаз и графит. Алмаз представляет собой однородную кристаллическую решетку, где каждый углеродный атом связан с четырьмя соседними атомами, образуя кубическую структуру. Благодаря этой структуре, алмаз обладает высокой твердостью и блеском.
Графит, в отличие от алмаза, имеет слоистую структуру, где углеродные атомы связаны между собой в плоскостях. Каждый атом связан с тремя соседними атомами, образуя особый шестиугольниковый узор. Благодаря такой структуре, графит обладает свойством быть мягким и смазочным материалом.
Однако, алмаз и графит - только два основных аллотропных состояния углерода. Огромное разнообразие углеродных аллотропов еще не до конца изучено. К ним относятся наличие углерода в аморфном состоянии, фуллерены, нанотрубки, графен и многое другое.
Фуллерены - это молекулы углерода, которые образуют полые сферические структуры. Они имеют уникальные свойства и широкое применение в научных и промышленных исследованиях. Нанотрубки - это цилиндрические структуры, состоящие из стенок, образованных углеродными атомами. Они представляют интерес для различных областей технологий, например, электроники и энергетики.
Графен - это двумерный кристалл, состоящий из одного слоя атомов углерода. Он обладает уникальными электронными и механическими свойствами, что делает его перспективным материалом для новых технологий и приложений.
Таким образом, углеродные аллотропы представляют собой неисчерпаемый источник интереса и исследований для ученых. Их разнообразие и уникальные свойства открывают новые горизонты для развития науки и технологий.
Углеродные соединения: основа органической химии
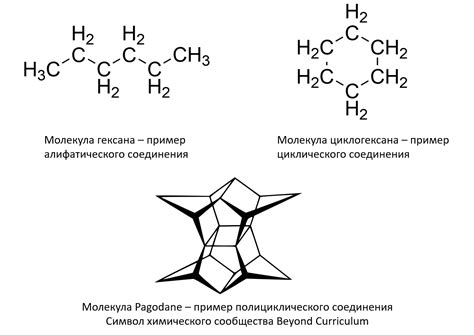
Органическая химия изучает углеродные соединения, которые включают в себя молекулы, состоящие из атомов углерода и других элементов, таких как водород, кислород, азот, сера и многих других. Углеродные соединения могут быть газообразными, жидкими или твердыми веществами, иметь разнообразные свойства и использоваться в широком спектре промышленных и научных областей.
Атомы углерода могут образовывать ковалентные связи с другими атомами углерода и различными элементами, что позволяет создавать огромное количество углеродных структур. Каждый атом углерода может образовывать четыре связи, что обеспечивает его высокую способность к образованию различных соединений.
Углеродные соединения могут быть простыми или сложными. Простые углеродные соединения включают такие соединения, как метан, этан, пропан и бутан. Сложные углеродные соединения могут включать множество атомов углерода, образуя длинные цепочки и сложные структуры.
Углеродные соединения также имеют разнообразные свойства, такие как способность к горению, растворимость в различных растворителях, реакционная активность и многие другие. Именно благодаря этим свойствам углеродные соединения нашли применение в таких сферах, как медицина, пищевая промышленность, электроника и материаловедение.
Универсальный работник: применение углерода в различных отраслях
- Энергетика: углерод используется в производстве электродов для батарей и аккумуляторов, что позволяет получить более высокую энергоемкость и длительность работы.
- Промышленность: углеродные волокна применяются при производстве легких и прочных материалов, например, для производства композитных материалов в авиационной и автомобильной промышленности.
- Медицина: углерод используется для создания различных имплантатов и протезов, благодаря своей прочности, устойчивости к коррозии и биосовместимости с тканями человека.
- Электроника: углеродные нанотрубки входят в состав различных электронных компонентов, таких как транзисторы и солнечные батареи, обладающие высокой электропроводностью и полупроводниковыми свойствами.
- Очистка воды и воздуха: углерод используется в процессах фильтрации для удаления загрязнений и вредных веществ из воды и воздуха.
Таким образом, углерод – это настоящий универсальный работник, который находит применение в самых различных отраслях и играет важную роль в нашей современной жизни.