Фосфор является одним из самых распространенных элементов в природе и играет важную роль в живых организмах. В периодической системе элементов отмечается его положение среди неметаллов, и благодаря этому фосфор обладает уникальными свойствами.
Одним из основных неметаллических свойств фосфора является его низкая проводимость электричества и тепла. Поэтому фосфор применяется в качестве изоляционного материала, например, в производстве оксидов фосфора путем восстановления фосфата аммония. Кроме того, его слабая проводимость является одним из факторов, обусловливающих его неметаллическую природу.
Фосфор обладает химической инертностью по сравнению с некоторыми другими неметаллами. Это свойство определяется низкой активностью фосфора в химических реакциях, особенно с водой и кислородом. Благодаря этому фосфор широко применяется в производстве множества химических соединений, таких как фосфиды и оксиды фосфора, которые находят широкое применение в различных отраслях промышленности.
Однако неметаллические свойства фосфора не такие слабые, как может показаться на первый взгляд. Он отличается высокой химической активностью и образует различные соединения с многими элементами. Например, фосфор образует гидриды, галогениды и множество кислотных и оксидных соединений. Именно благодаря этим свойствам фосфор находит широкое применение в сельском хозяйстве, медицине, производстве огнетушителей и других сферах деятельности.
Собственные свойства фосфора: как они отличаются от других элементов?

Высокая реакционность. Фосфор имеет способность образовывать соединения с большим количеством элементов. Он может образовывать соединения с металлами, неметаллами и даже другими фосфорными соединениями.
Тройственная валентность. Одним из наиболее характерных свойств фосфора является его тройственная валентность. Это означает, что он может образовывать соединения, в которых на один атом фосфора приходится три атома другого элемента.
Фосфоресценция. Фосфор обладает свойством фосфоресцировать, то есть излучать свет при воздействии на него определенной длины волн. Это свойство делает фосфор не только интересным для научных исследований, но и находит широкое применение в различных областях, включая светодиоды и солнечные батареи.
Фосфорные соединения. Фосфор образует огромное количество соединений с другими элементами. Некоторые из них обладают значительным значением в промышленности и науке. Например, фосфорные соединения широко используются в производстве удобрений, пестицидов и фармацевтических препаратов.
Все эти собственные свойства фосфора делают его одним из наиболее интересных элементов. Они позволяют использовать его в различных областях, от химической промышленности до биологических исследований, и продолжают привлекать внимание ученых и инженеров со всего мира.
Физические свойства фосфора: чем отличается от других элементов?

Одной из примечательных особенностей фосфора является его низкая температура плавления - всего лишь 44,1 градуса Цельсия. Это делает его одним из немногих элементов, плавящихся при комнатной температуре. При этом фосфор имеет высокую температуру кипения - 280 градусов Цельсия.
Фосфор также обладает высокой плотностью, равной 1,82 г/см³. Это делает его одним из самых плотных элементов, что придает ему важные применения в различных отраслях промышленности.
Еще одним интересным физическим свойством фосфора является его прозрачность для долговолнового ультрафиолетового излучения. Это свойство позволяет использовать фосфор в производстве экранов, светоизлучающих диодов и других электронных устройств.
| Свойство | Значение |
|---|---|
| Температура плавления | 44,1 °C |
| Температура кипения | 280 °C |
| Плотность | 1,82 г/см³ |
Таким образом, фосфор обладает уникальными физическими свойствами, которые делают его важным и интересным элементом во многих областях науки и промышленности.
Химические свойства фосфора: особенности и отличия от других элементов
Одним из основных отличий фосфора является его высокая реактивность. В атмосфере фосфор быстро окисляется и образует фосфаты, что делает его токсичным и взрывоопасным в некоторых формах. Это свойство делает его важным компонентом многих химических соединений и реакций.
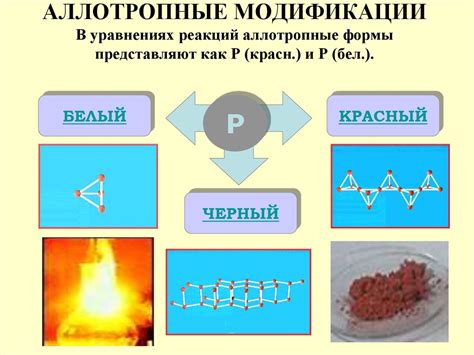
Примечательной особенностью фосфора является его способность образовывать различные аллотропные модификации. Он может существовать в нескольких формах, включая белый, красный и черный фосфор. Каждая форма обладает различными физическими и химическими свойствами, что делает фосфор уникальным элементом в периодической системе элементов.
Другой важной особенностью фосфора является его роль в биологических системах. Он является одним из основных компонентов нуклеиновых кислот и фосфолипидов, которые являются основными структурными элементами клеток. Фосфор также играет важную роль в энергетическом обмене организма, участвуя в процессе аденозинтрифосфата (АТФ) - основного источника энергии в клетках.
Особые химические свойства фосфора также проявляются в его способности образовывать соединения с другими элементами, такими как кислород, водород, азот и многие другие. Фосфор может образовывать различные органические и неорганические соединения, включая фосфаты, фосфориты, фосфиды и многое другое. Благодаря этому, фосфор широко используется в промышленности, сельском хозяйстве, медицине и других областях.
Биологические свойства фосфора: важность и влияние на живые организмы
Важность фосфора в организме
Фосфор является составной частью многих биологически активных веществ, таких как ДНК и РНК, аденозинтрифосфат (АТФ), фосфолипиды и фосфопротеины. Он необходим для синтеза нуклеиновых кислот и белков, участвует в передаче генетической информации и регуляции метаболических процессов.
Влияние фосфора на рост и развитие
Фосфор играет важную роль в росте и развитии живых организмов. Он необходим для нормального формирования костей и зубов, а также для нейронного развития. Благодаря своим свойствам, фосфор способствует образованию каркаса клеток, укреплению мембран и увеличению прочности тканей.
Участие фосфора в энергетических процессах
Фосфор играет ключевую роль в передаче энергии в клетках. Он является неотъемлемой частью молекулы АТФ – основного носителя энергии в организмах. АТФ образуется в результате окисления органических веществ и обеспечивает энергетические потребности клеток, необходимые для синтеза биологически активных веществ, работы мышц и обмена веществ в организме.
Роль фосфора в регуляции pH и буферной системы
Фосфор также является важным компонентом буферной системы организма. Он участвует в регуляции pH внутриклеточной и межклеточной среды, поддерживая оптимальные условия для функционирования ферментов и биологических процессов. Благодаря своим свойствам, фосфор помогает поддерживать стабильность внутренней среды организма в широком диапазоне внешних условий.
Фосфор является незаменимым элементом для жизни и здоровья всех организмов. Его слабые неметаллические свойства играют важную роль в реализации его биологической функции. Без них невозможно обеспечение энергетических потребностей организма, синтез биологически активных веществ и нормальное функционирование клеток.