Молекулярная и атомная масса – это понятия, которые часто встречаются в химических и физических изысканиях. Они имеют важное значение для понимания свойств и реакций веществ. Молекулярная масса относится к массе одной молекулы соединения, в то время как атомная масса связана с массой одного атома химического элемента.
Молекулярная масса определяется суммой атомных масс всех атомов в молекуле. Обычно выражается в атомных массовых единицах (аму) или в г/моль. Молекулярную массу можно найти путем сложения атомных масс каждого атома в молекуле. Например, для воды (H2O), молекулярная масса будет равна сумме атомных масс 2 атомов водорода и 1 атома кислорода.
Атомная масса – это средняя масса атома химического элемента, учитывая все изотопы элемента и их относительное распределение в природе. Атомная масса обычно выражается в атомных массовых единицах (аму) или в г/моль. Для большинства элементов атомная масса указана в периодической системе элементов. Например, атомная масса кислорода равна примерно 16 аму.
Молекулярная масса: определение и значение
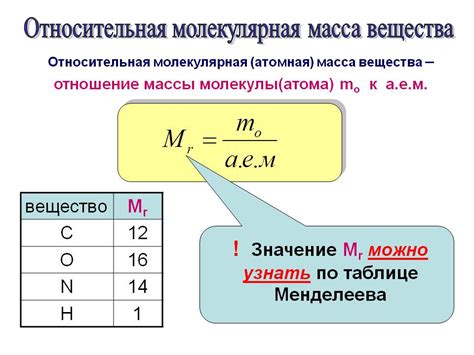
Молекулярная масса играет важную роль в химии, так как позволяет определить количество вещества на основе его массы. Это позволяет проводить точные расчеты при изучении химических реакций и взаимодействий веществ.
Для определения молекулярной массы необходимо знать атомные массы всех атомов в молекуле и их количество. Атомные массы указываются в периодической системе химических элементов.
Например, для молекулы воды (H2O) молекулярная масса будет равна сумме масс атома водорода (H) и двух атомов кислорода (O). С учетом атомных масс водорода (1,01 amu) и кислорода (16 amu), молекулярная масса воды будет равна 18,02 amu.
Знание молекулярной массы позволяет определить такие химические понятия, как молярная масса, количество вещества и стехиометрические расчеты. Она также используется для идентификации и классификации химических соединений.
Что такое молекулярная масса?

Молекулярная масса является суммой атомных масс всех атомов, составляющих молекулу. Для определения молекулярной массы необходимо знать химическую формулу соединения и атомные массы элементов, входящих в молекулу.
Чтобы найти молекулярную массу соединения, необходимо умножить количество атомов каждого элемента на его атомную массу и сложить полученные значения. Например, для воды (H2O) молекулярная масса будет равна (2 * масса атома водорода) + (1 * масса атома кислорода).
Молекулярная масса позволяет определить количество вещества в молях по известной массе, а также проводить расчеты на молекулярном уровне. Это важный параметр в химии, используемый для определения концентрации вещества, стехиометрических расчетов и других задач.
Для удобства сравнения молекулярных масс различных соединений приняты относительные молекулярные массы, которые выражаются в г/моль. Относительная молекулярная масса соединения равна молекулярной массе, выраженной в граммах, деленной на 1 моль этого соединения.
Измерение молекулярной массы производится с использованием различных методов, включая масс-спектрометрию и определение через известные величины, такие как плотность и бромовзрывную способность. Точное измерение молекулярной массы позволяет провести химическую и физическую характеристику соединения, его структурное и элементный составы.
| Примеры молекулярных масс некоторых соединений: | Молекулярная масса (г/моль) |
|---|---|
| Метан (CH4) | 16,04 |
| Ацетон (C3H6O) | 58,08 |
| Формальдегид (CH2O) | 30,03 |
Значение молекулярной массы в химии
Значение молекулярной массы может быть использовано для различных расчетов в химии, таких как определение количества вещества, молярной массы или молярного объема. Она позволяет оценить, сколько вещества содержится в данном образце или реакции, что необходимо для проведения тех или иных химических процессов.
Чтобы определить молекулярную массу данного соединения, необходимо знать атомные массы его составляющих элементов и их количество в молекуле. После чего атомные массы перемножаются на их количество и складываются. Результатом будет число, выраженное в атомных единицах массы (аму) или граммах на моль (г/моль).
Молекулярная масса может быть полезной как для определения химической формулы соединения, так и для выявления ионов и других реакционных продуктов. Она также может быть полезной в изучении структуры молекулы и предсказании ее свойств и реакционной активности.
Поэтому знание молекулярной массы является важным инструментом для химиков при проведении и анализе химических исследований. Она позволяет понять, какие изменения будут происходить веществе при взаимодействии с другими веществами и какова будет степень их воздействия.
Атомная масса: что это и как определить?
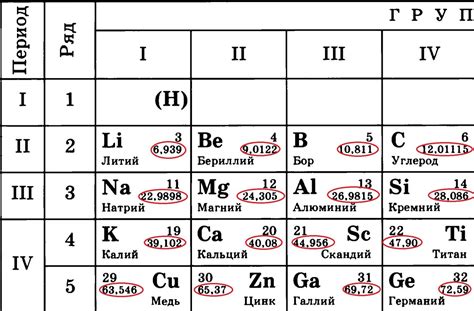
Определение атомной массы проводится с помощью специальных приборов и методов, таких как масс-спектрометрия. Масс-спектрометрия позволяет измерить массу атомов путем разделения их по отношению заряда и массы в магнитном поле.
Существует два метода определения атомной массы: прямой и косвенный. Прямой метод основан на измерении массы одного атома вещества и ее сравнении с известной массой другого элемента. В косвенном методе атомная масса вычисляется на основе массового распределения изотопов элемента и их относительной абундантности.
Важно отметить, что атомная масса может быть различной для разных изотопов химического элемента. Изотопы имеют одинаковое количество протонов в ядре, но различающееся число нейтронов, что приводит к различной атомной массе.
Что такое атомная масса?
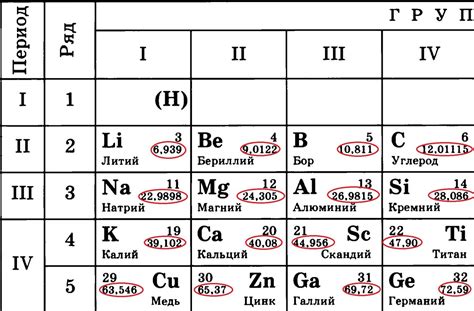
Атомная масса измеряется с помощью массового спектрометра, который позволяет определить массу исследуемого атома. Основной единицей измерения атомной массы является унифицированная атомная единица массы (а.е.м.), равная 1/12 массы атома углерода-12.
Масса атома складывается из его ядра и электронов, однако масса электронов пренебрежимо мала по сравнению с массой ядра, поэтому атомная масса практически равна массе ядра. Масса ядра, в свою очередь, находится по формуле: сумма числа протонов и нейтронов, умноженная на массу протона или нейтрона.
| Элемент | Атомная масса (а.е.м.) |
|---|---|
| Водород | 1.01 |
| Гелий | 4.00 |
| Углерод | 12.01 |
Атомная масса играет важную роль в химических расчетах, так как позволяет определить количество атомов вещества и производить массовые пропорции при реакциях. Важно отметить, что атомная масса может быть различной для изотопов одного элемента, так как они имеют разное количество нейтронов в ядре. Таким образом, атомная масса является уникальной характеристикой каждого отдельного элемента.
Как определяется атомная масса?

Определение атомной массы включает использование двух основных методов: масс-спектрометрии и химического анализа. Масс-спектрометрия основана на разделении ионов по их относительным массам и измерении их отклонения под воздействием электрического или магнитного поля. Этот метод позволяет определить массу атомов и молекул с высокой точностью.
Химический анализ, с другой стороны, основан на измерении количества вещества, взятого в эксперименте, и количества продукта реакции. Используя коэффициенты реакции, можно рассчитать отношение масс веществ и определить атомную массу атомов вещества.
Для определения относительной атомной массы изотопов используется метод массового спектрометра. Этот метод основан на разделении ионов, полученных из атомов изотопов, и измерении их относительных масс. Таким образом, атомная масса определенного изотопа может быть рассчитана и использована для определения общей атомной массы вещества с учетом ее изотопического состава.
Отличия молекулярной и атомной массы

Атомная масса относится к массе одного атома элемента. Она измеряется в атомных единицах массы (аму). Атомная масса определяется с использованием массы и относительных атомных масс всех изотопов данного элемента. Один атом углерода, например, имеет атомную массу приблизительно равную 12 аму.
С другой стороны, молекулярная масса относится к массе молекулы соединения. Она также измеряется в атомных единицах массы (аму) и является суммой атомных масс всех атомов в молекуле. Для примера, молекулярная масса воды (H2O) равна сумме атомных масс двух атомов водорода и одного атома кислорода, что составляет около 18 аму.
Таким образом, основное отличие между атомной и молекулярной массой состоит в измерении: атомная масса - это масса одного атома элемента, а молекулярная масса - это масса молекулы соединения, состоящей из двух или более атомов различных элементов.
Знание атомной и молекулярной массы важно для понимания реакций и свойств веществ. Атомная масса позволяет вычислить количество атомов вещества, а молекулярная масса позволяет определить количество молекул вещества на основе массы.
Чем отличается молекулярная масса от атомной?

Атомная масса относится к массе одного атома элемента в его естественно встречающемся состоянии. Она измеряется в атомных единицах массы (аму) и обычно указывается после символа элемента в таблице периодических элементов. Атомная масса рассчитывается на основе относительных атомных масс изотопов элемента и их пропорций в естественной смеси. Например, для углерода атомная масса составляет около 12,01 аму.
С другой стороны, молекулярная масса относится к массе одной молекулы вещества и измеряется также в атомных единицах массы. Молекулярная масса рассчитывается путем сложения атомных масс атомов, составляющих молекулу. Например, для молекулы воды (H2O) молекулярная масса равна приблизительно 18,02 аму, где 2 атома водорода имеют атомную массу около 1,01 аму каждый, а атом кислорода - около 16,00 аму.
Таким образом, атомная масса относится к массе одного атома элемента, тогда как молекулярная масса относится к массе молекулы вещества. Они играют важную роль в химических расчетах и позволяют определить количество вещества на основе его массы.