Каталаза - это фермент, играющий важную роль в биологических процессах организма. Этот фермент участвует в разложении перекиси водорода, являющейся побочным продуктом метаболизма клеток.
Каталаза относится к классу оксидоредуктазы и является одним из самых распространенных ферментов в живой природе. Она катализирует реакцию, в результате которой перекись водорода распадается на молекулу воды и кислород. Этот процесс необходим для очистки организма от токсичной перекиси водорода, образующейся при метаболических процессах.
Особенностью каталазы является ее эффективная работа в присутствии низких концентраций вещества. Кроме того, каталаза способна работать при различных pH-условиях. Эти свойства позволяют ей выполнять свою функцию в различных организмах и тканях.
Каталаза играет важную роль в жизни организмов. Она защищает клетки от повреждений, вызванных активными формами кислорода, и помогает поддерживать внутреннюю среду организма в состоянии гомеостаза. Изучение каталазы на уроках биологии в 8 классе позволяет учащимся понять значение этого фермента в жизнедеятельности.
История открытия каталазы
В своих экспериментах Пастер выяснил, что каталаза присутствует в большинстве организмов, включая растения, животных и микроорганизмы. Кроме того, Пастер показал, что каталаза обладает высокой активностью и эффективно справляется с разложением пероксида водорода, который является токсичным продуктом обмена веществ.
Открытие каталазы имело важные практические последствия. Каталаза была применена в медицине для лечения ран, облученных радиацией. Также каталаза используется в пищевой промышленности для стабилизации цвета пищевых продуктов и предотвращения окисления.
Исторический обзор

История изучения каталазы в биологии началась в XIX веке. Значительный вклад в ее исследование внесли такие ученые, как Луи Пастер, Людвиг Онтрайер, Ода Ауслав и многие другие. Они стали первыми, кто установил связь между наличием каталазы в организмах и их способностью разлагать водород пероксид.
Великолепие каталазы обнаружилось значительно позже, когда Хакан и Болли изолировали и характеризовали этот уникальный фермент. Они обнаружили, что каталаза обладает способностью активировать водород пероксид с возможностью его разрушения на безвредные молекулы воды и кислорода.
| Год | Открытие |
|---|---|
| 1818 | Первые наблюдения за феноменом разложения водород пероксида |
| 1863 | Изображение каталазы в живых организмах |
| 1900 | Открытие и характеристика каталазы |
| 1948 | Изучение механизмов работы каталазы |
С тех пор исследования каталазы только усилились, и ее роль в биологических системах стала лучше понята. Сегодня каталаза является одним из самых хорошо изученных ферментов и используется в различных областях исследования, в том числе в медицине, пищевой промышленности и окружающей среде.
Структура и функции каталазы
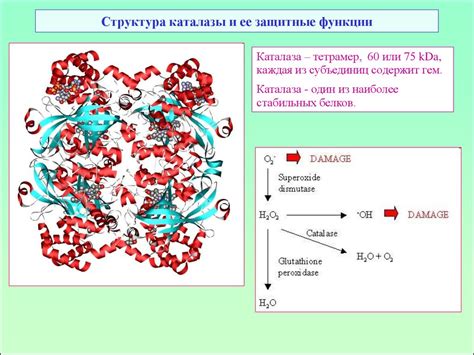
Структура каталазы состоит из белка, имеющего геминовый группу в активном центре. Это позволяет ей взаимодействовать с перекисью водорода и ускорять ее разложение на воду и кислород.
Функции каталазы связаны с защитой клеток от негативных эффектов перекисного окисления. Перекись водорода может быть опасной для клеток, так как она может повреждать биомолекулы, включая ДНК, РНК и белки. Каталаза помогает предотвратить такие повреждения, разлагая перекись водорода на недопустимые компоненты.
Кроме того, каталаза также играет важную роль в процессе дыхания. Она участвует в разложении перекиси водорода, которая образуется в процессе окисления глюкозы или других органических соединений, и предотвращает токсическое воздействие перекиси на клетки.
Структура фермента
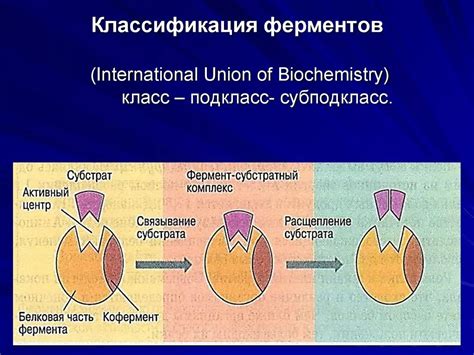
Фермент каталаза содержит несколько подединиц, каждая из которых состоит из белковых цепочек. Такая структура позволяет ферменту быть достаточно устойчивым и эффективным в катализе реакции. Активный центр фермента обладает специальными аминокислотными остатками, которые взаимодействуют с молекулами перекиси водорода и обеспечивают проведение катализируемой реакции.
| Подединицы | Аминокислотные остатки | Функция |
|---|---|---|
| alpha-подединица | гистидины | катализ проведение водородной реакции |
| beta-подединица | глутаминовая кислота | стабилизация активного центра |
| gamma-подединица | лейцин, изолейцин | соединение с другими белками |
Структура фермента каталазы позволяет ему быть активным в разных условиях окружающей среды. Например, каталаза сохраняет свою активность при небольших изменениях температуры или рН.
Функции каталазы
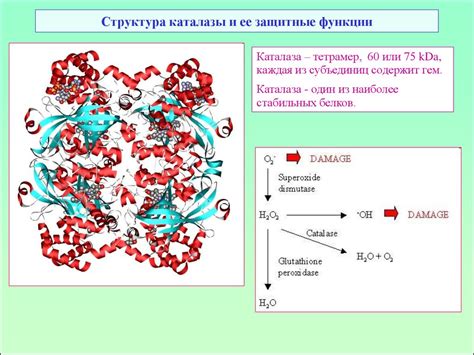
Основная функция каталазы заключается в защите клетки от вредного влияния перекиси водорода. Этот продукт окисления образуется во многих метаболических процессах и может накапливаться в клетке, что приводит к повреждению ее структуры и нарушению нормального функционирования.
Кроме того, каталаза играет роль в детоксикации организма. Она способна разлагать различные ядовитые вещества, такие как формальдегид и ацетальдегид, в безопасные продукты, что помогает организму очищаться от вредных соединений.
Другая важная функция каталазы - участие в биосинтезе гормонов и других биологически активных веществ. Она участвует в различных реакциях обмена веществ, которые приводят к образованию важных молекул для организма, таких как гормоны щитовидной железы и меланин.
Также каталаза играет роль в иммунной системе организма. Она участвует в уничтожении бактерий, вирусов и других патогенных микроорганизмов, которые попадают в организм через раны или слизистые оболочки. Каталаза разлагает перекись водорода, которая образуется при реакции иммунной системы на внешние агенты.
| Функции каталазы | Примеры задач |
|---|---|
| Защита клетки | Разложение перекиси водорода |
| Детоксикация организма | Разложение ядовитых веществ |
| Участие в биосинтезе | Синтез гормонов и других важных веществ |
| Участие в иммунной системе | Уничтожение бактерий и вирусов |
Механизм действия каталазы
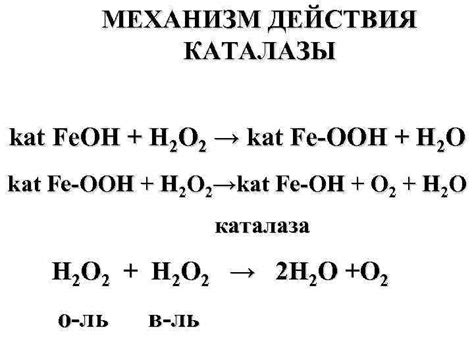
Механизм действия каталазы основан на специфической реакции, которая происходит в активном центре фермента. Активный центр - это участок каталазы, где происходит привязывание и преобразование субстрата. В случае с каталазой, субстратом является водородный пероксид.
Процесс действия каталазы можно разделить на несколько этапов:
- Инициация: молекула водородного пероксида связывается с активным центром каталазы.
- Окисление: активное центре фермента окисляет молекулу водородного пероксида, перенося электроны на другую молекулу или группу аминокислот, что приводит к образованию алкилиц.
- Разложение: алкиль возникает из активного центра каталазы и реагирует с другими алкилидами, что приводит к диссоциации водородного пероксида на воду и молекулярный кислород.
- Регенерация: активный центр каталазы возвращается к своему исходному состоянию и может принять новую молекулу водородного пероксида для дальнейшей обработки.
Механизм действия каталазы может быть описан как каскадная реакция, в которой катализатор (каталаза) ускоряет химическую реакцию, не расходуясь при этом. Этот процесс позволяет клеткам эффективно разлагать водородный пероксид, который является продуктом обмена веществ, и предотвращает накопление этого вещества, что может быть токсичным для организма.
Каталаза и нейтрализация водорода
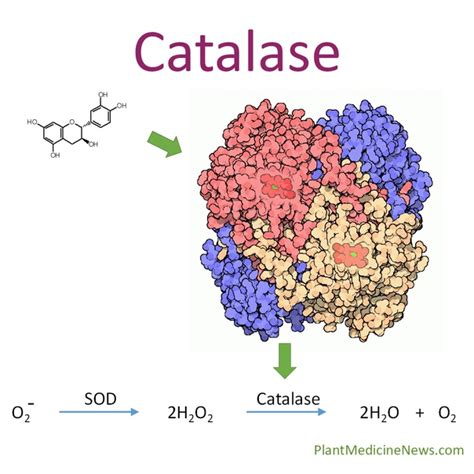
Функция каталазы заключается в том, чтобы предотвращать образование и накопление в клетках вредного для них водорода. В клетке происходят многочисленные химические реакции, в результате которых образуется водород. Если водород накапливается в клетке, это может привести к нарушению ее функции и даже разрушению. Каталаза играет ключевую роль в нейтрализации водорода, что помогает поддерживать нормальное функционирование клеток.
В процессе нейтрализации водорода каталаза преобразует перекись водорода в воду и кислород. Реакция выглядит следующим образом:
- H2O2 + каталаза -> H2O + O2
Таким образом, каталаза ускоряет разложение перекиси водорода на воду и кислород, обеспечивая эффективную нейтрализацию вредного продукта обмена веществ.
Каталаза присутствует в разных организмах - растениях, животных и бактериях. Она активно используется клетками для защиты от вредного воздействия водорода, а также участвует в других процессах, связанных с обменом веществ и защитой клеток от окислительного стресса.
Кинетика каталазы
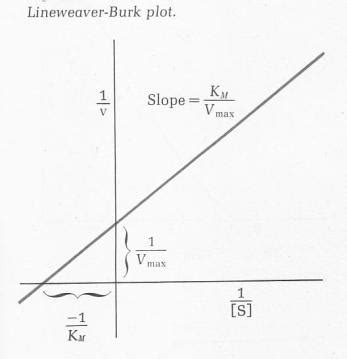
Кинетика каталазы изучает скорость энзиматической реакции и зависимость этой скорости от концентрации субстрата или других факторов.
Обычно, при измерении активности каталазы, используется концентрация водорода пероксида. При увеличении концентрации субстрата, скорость реакции сначала увеличивается до определенного предела, называемого максимальной скоростью или Vмакс. После достижения этого предела, скорость реакции перестает увеличиваться, так как все ферменты находятся в состоянии насыщения.
Существует несколько факторов, которые могут влиять на кинетику каталазы. Один из них - pH. Каталаза обычно работает при pH, близком к 7, но в зависимости от организма может быть активна при других значениях pH. Температура также существенно влияет на активность каталазы. При повышении температуры, ее активность обычно увеличивается, но только до определенного предела. При очень высоких температурах фермент может денатурироваться, теряя свою активность.
Таким образом, кинетика каталазы является сложным процессом, зависящим от различных факторов, таких как концентрация субстрата, pH и температура. Изучение кинетики позволяет более глубоко понять особенности работы этого важного фермента в организме.
Роль каталазы в организме
Перекись водорода образуется в клетках в результате метаболических процессов и является очень активным оксидантом. В больших количествах она может вызывать повреждения клеточных мембран, ДНК и белковых структур, что негативно сказывается на работе организма и может привести к различным заболеваниям.
Каталаза располагается в пероксисомах – мембранных органеллах, в которых происходит образование и разложение перекиси водорода. Благодаря активности каталазы пероксисомы играют важную роль в метаболических процессах и обезвреживании токсических веществ.
Каталаза также имеет значение для работы клеток иммунной системы. Она защищает фагоциты – клетки, поглощающие и уничтожающие бактерии и вирусы, от вредного воздействия перекиси водорода, которая образуется при фагоцитозе. Благодаря каталазе фагоциты могут более эффективно выполнять свою защитную функцию.
Каталаза представляет собой важный компонент антиоксидантной системы организма. Она сотрудничает с другими ферментами и молекулярными антиоксидантами, такими как супероксиддисмутаза и глутатионпероксидаза, создавая стабильный и сбалансированный антиоксидантный потенциал.
Благодаря каталазе организм может более эффективно защищаться от окислительного стресса, который возникает при повышенной концентрации перекиси водорода или других активных кислородсодержащих соединений.
Участие каталазы в метаболических процессах
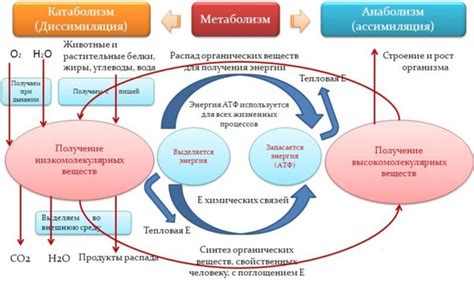
Водород перекиси (H2O2) является продуктом многих биохимических реакций в организмах. Но в больших концентрациях он может стать токсичным и нанести ущерб клеткам. Каталаза помогает предотвратить этот вред, катализируя разложение H2O2 на безопасные компоненты.
Этот процесс особенно важен в клетках, так как они производят H2O2 в процессе дыхания, окисления жирных кислот и других метаболических процессов. К счастью, в клетках также присутствует каталаза для разложения H2O2 и предотвращения его накопления.
Каталаза также играет важную роль в защите организма от внешних воздействий. Например, воспалительные процессы в организме могут приводить к повышенному образованию H2O2, и увеличение активности каталазы помогает нейтрализовать этот эффект.
Таким образом, каталаза является важным ферментом, обеспечивающим безопасность клеток и участвующим в регуляции метаболических процессов организма.
Влияние каталазы на здоровье

Перекись водорода – вещество, образующееся в организме как естественный продукт метаболических процессов. Однако, накопление перекиси водорода может стать причиной различных заболеваний и проблем со здоровьем. Каталаза, действуя как антиоксидант, снижает содержание перекиси водорода и защищает клетки организма от окислительного стресса.
Окислительный стресс – это состояние, когда неравновесие между образованием и устранением свободных радикалов приводит к повреждению клеток и тканей. Она может быть вызвана факторами, такими как стресс, загрязнение окружающей среды, неправильное питание и некоторые заболевания. Недостаточное количество каталазы или ее недостаточная активность может привести к увеличению уровня перекиси водорода и повышенному риску развития окислительного стресса.
Окислительный стресс может привести к различным заболеваниям, таким как сердечно-сосудистые заболевания, рак, диабет и артрит. Он также может усугубить уже существующие заболевания и ускорить процесс старения. Важно поддерживать баланс каталазы в организме, чтобы предотвратить накопление перекиси водорода и снизить риск развития окислительного стресса.
Существуют некоторые способы поддержания активности каталазы и минимизации окислительного стресса. Они включают в себя правильное питание, богатое антиоксидантами, регулярную физическую активность, достаточный сон, снижение стресса и избегание вредных привычек, таких как курение и употребление алкоголя. Эти меры помогут укрепить защиту организма от процессов окисления и сохранить хорошее здоровье.