Физический процесс и химическая реакция - это два ключевых концепта в науке о веществе. Оба процесса относятся к изменениям состояния вещества, но имеют существенные отличия.
Физический процесс - это физическое изменение состояния вещества, при котором не происходит образования новых веществ. В физических процессах изменяются физические свойства материала, такие как форма, размер, объем или агрегатное состояние, но его химический состав остается неизменным. Например, плавление льда или испарение воды - это физические процессы, поскольку вода остается веществом воды.
Химическая реакция - это процесс превращения одних веществ в другие. В результате химической реакции образуются новые химические соединения с уникальными свойствами. Химические реакции происходят за счет взаимодействия молекул вещества и изменения их химической структуры. Примером химической реакции является сжигание древесины, где древесина (углеводородное соединение) взаимодействует с кислородом и превращается в диоксид углерода и воду.
Таким образом, физические процессы отличаются от химических реакций тем, что они не приводят к образованию новых веществ с уникальными свойствами. В то же время, химические реакции изменяют химический состав вещества и образуют новые соединения. Понимание различий между этими процессами является важной основой для понимания многих аспектов науки о веществе и ее приложений в различных областях.
Основные отличия физического процесса от химической реакции
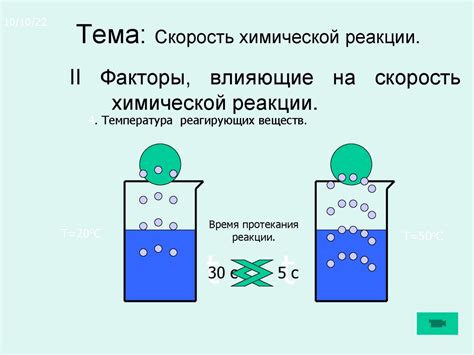
1. Изменение состава вещества: Физический процесс не ведет к изменению химического состава вещества, а химическая реакция приводит к образованию новых веществ с другим химическим составом.
2. Энергия: Физический процесс требует меньше энергии, чем химическая реакция. В химической реакции выполняется разрыв и/или создание химических связей, что требует большего количества энергии.
3. Обратимость: Физические процессы обычно обратимы, то есть исходное вещество может быть восстановлено в начальное состояние путем изменения условий, в то время как химические реакции часто являются необратимыми и окончательными.
4. Реакционная способность: Вещества, участвующие в физическом процессе, обычно не обладают реакционной способностью и не стремятся к образованию новых веществ, тогда как вещества, участвующие в химической реакции, реагируют между собой и образуют новые соединения.
5. Изменение свойств: Физический процесс может привести только к изменению физических свойств вещества, таких как температура, плотность, фазовые переходы и т.д. Химическая реакция, напротив, приводит к изменению химических свойств вещества, таких как его активность, степень окисления, кислотность и т.д.
Природа явлений

Физический процесс - это изменение состояния вещества без образования новых веществ. Внешний вид или свойства вещества могут меняться, но его состав остается неизменным. Примерами физических процессов являются плавление льда, испарение воды, сжатие газа и деформация тела.
Химическая реакция - это процесс, в результате которого происходит превращение одних веществ в другие. В ходе химической реакции образуются новые вещества с новыми свойствами. Примеры химических реакций включают горение древесины, окисление металлов и фотосинтез.
Основное отличие физического процесса от химической реакции заключается в изменении состава вещества. Если в процессе изменения сохраняется состав вещества, то это физический процесс. Если в процессе происходит образование новых веществ с измененным составом, то это химическая реакция.
- Физические процессы и химические реакции имеют различные причины и механизмы протекания.
- Физические процессы связаны с изменением физических свойств вещества, таких как температура, плотность или объем.
- Химические реакции имеют место при взаимодействии веществ и приводят к образованию новых веществ.
- Физические процессы могут быть обратимыми, тогда как химические реакции обратимыми не являются.
Таким образом, понимание природы физических процессов и химических реакций позволяет более глубоко познать законы природы и взаимодействия веществ в окружающей среде.
Изменение состава веществ
В химической реакции происходит изменение состава и структуры вещества. Это происходит путем образования или разрушения химических связей между атомами и молекулами. В результате химической реакции образуются новые вещества с совершенно другими свойствами, отличными от исходных.
Примеры изменения состава вещества в химической реакции можно найти во многих повседневных процессах. Например, сгорание древесины - это химическая реакция, при которой древесина окисляется кислородом и образуются новые вещества - углекислый газ и вода. Еще одним примером может служить ржавление металла, при котором железо и кислород реагируют, образуя ржавчину - новое вещество с совершенно иными свойствами.
Энергетические изменения:

Физический процесс обычно сопровождается меньшими энергетическими изменениями по сравнению с химической реакцией. В физическом процессе энергия не создается и не уничтожается, а только перемещается или превращается в другие формы.
В химической реакции энергетические изменения играют ключевую роль. Реагенты и продукты химической реакции содержат разную энергию связей между атомами и молекулами, что приводит к изменению общей энергии системы.
В химической реакции может происходить поглощение или выделение энергии. Если реакция происходит с поглощением энергии, то она считается эндотермической. При этом энергия поглощается из окружающей среды для активации реакции и образования продуктов. Если реакция сопровождается выделением энергии, то она считается экзотермической. При этом выделяющаяся энергия может быть в форме тепла, света или другой формы энергии.
Энергетические изменения в химических реакциях могут быть измерены с помощью различных методов, таких как калориметрия или спектроскопия. Это позволяет определить тепловой эффект реакции, который имеет важное значение при изучении химических процессов и разработке новых веществ и материалов.
Скорость протекания процессов

Физический процесс может происходить с различной скоростью, но он всегда протекает очень быстро, за малый промежуток времени. Например, изменение положения объектов, движение тела по прямой или по параболе - все это является физическими процессами, которые происходят очень быстро.
Химическая реакция, в свою очередь, имеет более низкую скорость протекания. Она происходит на уровне атомов и молекул, которые переходят из одного состояния в другое. Химические реакции могут быть очень быстрыми, например, взрыв или сгорание, но также могут происходить медленно, требуя значительного времени для завершения.
Скорость протекания химической реакции зависит от нескольких факторов, включая концентрацию реагентов, температуру, присутствие катализаторов и поверхности реагентов. Например, повышение концентрации реагентов и температуры может ускорить химическую реакцию.
Таким образом, скорость протекания процессов является одной из основных характеристик, которая различает физический процесс от химической реакции. Физический процесс происходит очень быстро, в то время как химическая реакция может быть как быстрой, так и медленной в зависимости от условий.
Обратимость процессов
Физические процессы характеризуются своей обратимостью, то есть могут происходить как в прямом, так и в обратном направлении. Например, при нагревании воды она превращается в пар, а при охлаждении пара вода конденсируется обратно. Это явление называется термодинамической обратимостью.
Химические реакции, в свою очередь, обладают разной степенью обратимости. Некоторые реакции проходят только в одном направлении и невозможно вернуться к исходным веществам. Например, реакция образования воды из водорода и кислорода является нереверсивной. Однако существуют химические реакции, которые могут протекать как в прямом, так и в обратном направлении в зависимости от условий. Такие реакции называются обратимыми.
Обратимые химические реакции обычно характеризуются равновесием, когда скорость прямой реакции становится равной скорости обратной. Такие реакции происходят в закрытой системе, где количество веществ остается постоянным, и достигается равнодействие между прямой и обратной реакцией.
Равновесие в обратимых химических реакциях может смещаться в зависимости от изменения температуры, давления или концентрации веществ. Это позволяет контролировать направление и скорость химических процессов, что является важным аспектом в области химии и промышленности.
Важно отметить, что обратимость процессов является одним из ключевых отличий между физическими процессами и химическими реакциями.
Значимость для жизни
Физические процессы и химические реакции играют важную роль в жизни нашего мира. Они обуславливают основные законы и принципы, которые определяют функционирование природных систем и организмов.
Физические процессы, такие как теплопроводность, кондукция и радиация, позволяют поддерживать тепло и энергетическое равновесие в природных системах. Они обеспечивают нормальное теплообменное взаимодействие между организмами и окружающей средой.
Химические реакции, с другой стороны, являются основой жизненно важных функций организмов. Это процессы, при участии которых продукты питания расщепляются для получения энергии, а также происходит синтез необходимых нуклеиновых кислот, белков и других органических соединений.
Присутствие химических реакций в организмах также позволяет поддерживать химическое равновесие, необходимое для жизнедеятельности. Это включает в себя регуляцию pH уровня внутри организмов, а также поддержание концентраций различных молекул на необходимом уровне.
Таким образом, как физические процессы, так и химические реакции играют важную роль в жизни организмов и природных систем. Понимание их принципов и взаимодействий помогает нам лучше понять и адаптироваться к окружающей среде, а также разрабатывать новые методы и технологии, которые позволяют нам улучшить качество жизни и сохранить нашу планету для будущих поколений.