Дейтерий и тритий - два изотопа водорода, очень важных для науки и различных прикладных сфер. Хотя оба этих изотопа являются радиоактивными, они отличаются от обычного водорода не только массой, но и своими свойствами.
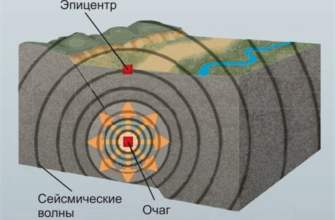
Дейтерий представляет собой изотоп водорода, состоящий из одного протона и одного нейтрона, что в два раза больше, чем у обычного водорода. Именно поэтому его масса также больше, и считается равной приблизительно 2 атомным массам. Дейтерий стабилен и относительно долго сохраняется в природе. Он широко используется в ядерной и плазменной физике, а также в качестве ядерного топлива в термоядерных реакторах.
Тритий, в свою очередь, является изотопом водорода, состоящим из одного протона и двух нейтронов. Масса трития является примерно втрое большей, чем у обычного водорода. Главное свойство трития - его высокая радиоактивность. Это свойство делает его опасным для здоровья человека, поэтому тритий используется в основном в научных исследованиях и в промышленности. Он служит важным компонентом в ядерных реакторах и водородных бомбах, а также при создании специальных источников света и прецизионных приборов.
Что такое дейтерий?
Понятие дейтерия стало известно в начале 20 века, когда исследователи обнаружили, что водород может иметь различные формы в зависимости от присутствия дейтерия. Дейтерий широко используется в ядерной физике и ядерной энергетике, так как его ядро можно использовать для синтеза тяжелых элементов и производства энергии через ядерные реакции.
Также дейтерий играет важную роль в астрофизике, поскольку его наличие или отсутствие в космических облаках может указывать на процессы, происходящие во Вселенной. Например, изучение изотопного состава дейтерия в космической пыли может помочь ученым понять, какие процессы приводят к образованию звезд и галактик.
Дейтерий также используется в медицине для создания технических устройств, например, в ядерных магнитно-резонансных томографах (МРТ), которые используются для диагностики и исследования различных заболеваний.
Интересно отметить, что дейтерий также может быть найден в природе в виде трития - радиоактивного изотопа водорода, состоящего из одного протона и двух нейтронов. В отличие от дейтерия, тритий является нестабильным и распадается со временем.
В целом, дейтерий является важным исследовательским и практическим инструментом в различных областях науки и технологий.
Определение дейтерия и его свойства

Дейтерий имеет ряд уникальных свойств, которые отличают его от обычного водорода:
- Масса. Масса дейтерия в два раза больше, чем у протия. Это связано с наличием дополнительного нейтрона в ядре.
- Стабильность. Дейтерий является стабильным изотопом с длительным сроком полураспада. Это делает его полезным для многих физических и химических исследований.
- Возможность ядерных реакций. Дейтерий используется в ядерных реакциях и термоядерных реакторах для получения энергии. При этом, при соединении с другим изотопом водорода – тритием, образуется гелий и высвобождается огромное количество энергии.
- Коррозионная стойкость. Дейтерий имеет более низкую активность по отношению к металлам, поэтому материалы, контактирующие с дейтерием, обычно менее подвержены коррозии.
- Использование в медицине. Дейтерий используется в качестве метки в лекарственных препаратах и молекулярной биологии для исследования физиологических процессов в организме.
Из-за своих особых свойств, дейтерий является объектом широких научных исследований и находит применение в различных областях науки и техники.
Применение дейтерия в научных и практических целях

Дейтерий, изотоп водорода с атомным номером 2 и массовым числом 2, имеет ряд уникальных свойств, что делает его полезным в научных и практических областях.
Одним из наиболее распространенных применений дейтерия является использование его в ядерных реакциях. Дейтерий используется в ядерных реакторах для получения энергии. При этом происходит слияние атомов дейтерия, что сопровождается выделением большого количества энергии. Данный процесс используется в термоядерных реакторах, которые позволяют получать энергию из ядерного синтеза. Также дейтерий используется в ядерных реакциях для получения радиоактивных изотопов.
Дейтерий также широко используется в научных исследованиях. Использование дейтерия позволяет исследовать химические и физические свойства веществ, а также изучать структуру и динамику биологических молекул. Изотопный эффект дейтерия является одним из важнейших средств для исследования различных процессов в физике, химии и биологии.
Помимо этого, дейтерий применяется в медицине. Например, дейтерированная вода (вода, содержащая повышенное количество дейтерия) используется в некоторых медицинских процедурах, таких как исследование обмена веществ и изучение мозговой активности при помощи методов исследования магнитно-резонансной томографии.
Таким образом, дейтерий играет важную роль в науке и практике. Его уникальные свойства позволяют использовать его для получения энергии, проведения научных исследований и различных медицинских процедур.
Что такое тритий?
Тритий используется в различных отраслях, включая ядерную энергетику и ядерные исследования. Он широко применяется в водородных бомбах и для увеличения эффективности ядерных реакторов. Тритий также используется в медицине для обозначения пути потока жидкости и для маркировки различных веществ.
Из-за своей радиоактивности тритий является опасным для жизни и здоровья человека. При попадании в организм он может нанести вред органам и вызвать раковое заболевание. Поэтому тритий требует особых условий хранения и обращения.
| Характеристики трития | Значение |
|---|---|
| Массовое число | 3 |
| Атомный номер | 2 |
| Масса атома | 3,0160492777 атомных масс |
| Период полураспада | 12,32 лет |
| Источники | Производство в ядерных реакторах или с помощью ускорителей частиц |
Определение трития и его свойства

- Тритий является радиоактивным изотопом и испускает бета-частицы в процессе радиоактивного распада.
- Изотоп трития обладает тремя различными формами состояния – газообразной, жидкой и твердой. В газообразной форме тритий обладает свойствами, подобными обычному водороду, но обладает большей плотностью. В жидкой форме тритий является веществом, обладающим свойствами радиоактивной воды. В твердой форме тритий образует кристаллическую решетку.
- Тритий является ключевым компонентом в термоядерных реакциях, таких как термоядерный синтез, который происходит в Солнце и других звездах.
- Экспозиция трития может быть опасной для здоровья человека, так как он проникает в организм через пищеварительную систему, легкие и кожу. Постоянная экспозиция тритию может привести к изменениям в ДНК и другим формам радиационного повреждения.