Конспект по химии 8 класс – это компактная запись основных тем и понятий, изучаемых восьмиклассниками на уроках химии. Он помогает ученику систематизировать и запомнить материал, а также углубить свои знания в этой науке. Конспект позволяет легко повторить пройденный материал перед контрольной работой или экзаменом, а также использовать его в качестве подготовки к урокам и домашним заданиям.
Конспект по химии 8 класс может содержать различную информацию, такую как определения понятий, примеры решения задач, химические реакции, таблицы и формулы. Важно уметь выделить основное, удалить ненужную информацию и описывать темы в своих словах.
Составление конспекта помогает ученику оставаться внимательным и фокусироваться на информации, подробно разбирая каждую тему. Это также развивает навык самостоятельного изучения, умение выделять главное от второстепенного.
Основные понятия и определения

В химии 8 класса основные понятия и определения играют важную роль. Ниже приведены основные термины и их определения, которые помогут ученику лучше понять материал урока.
| Термин | Определение |
|---|---|
| Вещество | Вещество - это форма материи, которую можно ощущать прикосновением, а также имеющая массу и объем. |
| Состав вещества | Состав вещества - это характеристика, которая указывает, из каких элементов и в каком соотношении состоит данное вещество. |
| Элемент | Элемент - это вещество, которое нельзя разложить на более простые вещества путем химических реакций. |
| Соединение | Соединение - это вещество, образованное двумя или более элементами, объединенными в определенном соотношении. |
| Химическая формула | Химическая формула - это символьное обозначение соединения, состоящее из символов элементов и индексов, указывающих на количество атомов каждого элемента. |
| Молекула | Молекула - это наименьшая частица соединения, обладающая его характеристиками и состоящая из двух или более атомов. |
История развития химии
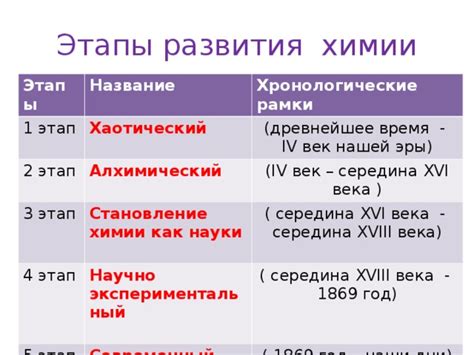
Первые шаги в изучении химических явлений были сделаны древними греками и египтянами. Они обладали знаниями о некоторых химических веществах и процессах, таких как известняк, сера и пектина. Эти знания были в значительной степени эмпирическими и не были систематизированы.
В средние века развитие химии было связано с алхимией - древней практической наукой, основанной на идеях о превращении материи и поиске философского камня, который предполагался способным превращать любые металлы в золото.
В 17 и 18 веках химия претерпела существенные изменения. В это время были сделаны открытия о законах сохранения массы и энергии, а также об элементах вещества. Джозеф Блэк открыл существование углекислого газа, Джозеф Прюст предложил закон постоянства состава химического соединения.
С начала 19 века химия стала развиваться в качестве науки. Джон Дальтон разработал теорию атомов, Михаил Ломоносов провел исследования в области химических реакций, Авогадро установил число, которое стало известно как число Авогадро.
В 20 веке химия стала еще более развитой наукой. Открытие радиоактивности, структуры атома, развитие органической химии - все это стало возможным благодаря работе таких ученых, как Мария и Пьер Кюри, Дмитрий Менделеев, Луи Пастер и многих других.
| Период | Ученые |
|---|---|
| Древний мир | Гиппократ, Демокрит, Птолемей, Галиен |
| Средние века | Аль-Химия (Аль-Газали, Аль-Рази, Парацельс) |
| 17-18 века | Роберт Бойль, Шарль Кулон, Антуан Лавуазье, Джозеф Прюст |
| 19 век | Джон Дальтон, Михаил Ломоносов, Авогадро |
| 20 век | Мария и Пьер Кюри, Дмитрий Менделеев, Луи Пастер |
Структура атома и периодическая система элементов

Ядро атома содержит протоны и нейтроны. Протоны имеют положительный заряд, а нейтроны – не имеют заряда. Общий заряд ядра определяет химические свойства элемента и называется атомным номером. Он указывает, сколько электронов находится в атоме и определяет его положение в периодической системе элементов.
Вокруг ядра атома движутся электроны по строго определенным орбитам, образуя электронную оболочку. Количество электронов в атоме равно количеству протонов в ядре и определяет электрическую нейтральность атома.
Периодическая система элементов – это систематическое упорядочение химических элементов по возрастанию атомного номера. Она представляет собой таблицу, в которой элементы расположены по горизонталям и вертикалям, называемым периодами и группами. Периоды соответствуют количеству электронных оболочек, а группы – количеству электронов на внешней энергетической оболочке. Периодическая система элементов помогает систематизировать знания о химических свойствах и использовании различных элементов.
Каждому химическому элементу в периодической системе присваивается символ, состоящий из одной или двух латинских букв. Например, H – водород, He – гелий, C – углерод, Fe – железо и так далее.
Структура атома и периодическая система элементов являются основами химии и позволяют понять строение и свойства вещества.
Химические реакции и их классификация
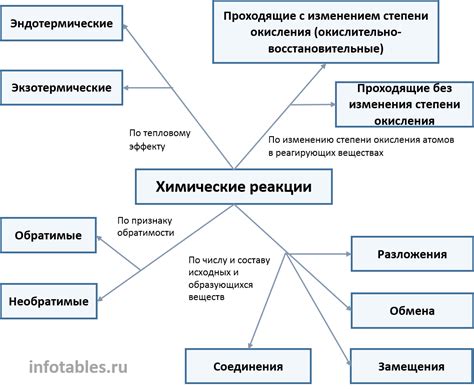
Химические реакции можно классифицировать по разным признакам. Рассмотрим некоторые основные классификации:
- По типу взаимодействующих веществ:
- Синтез (сложение) - при этом типе реакции два или несколько веществ объединяются, образуя новое вещество. Примером такой реакции может служить образование воды из водорода и кислорода.
- Анализ (расщепление) - это обратный процесс к синтезу, при котором одно вещество разлагается на два или более продукта. Например, разложение воды на водород и кислород.
- Замещение - при этом типе реакции атомы или группы атомов одного вещества замещают атомы или группы атомов другого вещества. Примерами могут служить реакции образования хлорида натрия из хлора и натрия, или реакция образования серы из железного воска.
- Обратимые и необратимые реакции - обратимые реакции могут протекать в обе стороны, то есть продукты могут опять превратиться в исходные вещества при изменении условий реакции. Необратимые реакции, наоборот, не могут проходить в обратном направлении.
- Быстрые реакции - реакции, которые протекают очень быстро. Примерами могут служить взрывы или горение.
- Медленные реакции - реакции, которые протекают очень медленно. Например, окисление металла в течение длительного времени.
Наличие знаний о классификации химических реакций позволяет лучше понимать, как происходят эти реакции, и использовать эту информацию в различных областях науки и промышленности.
Особенности химических элементов
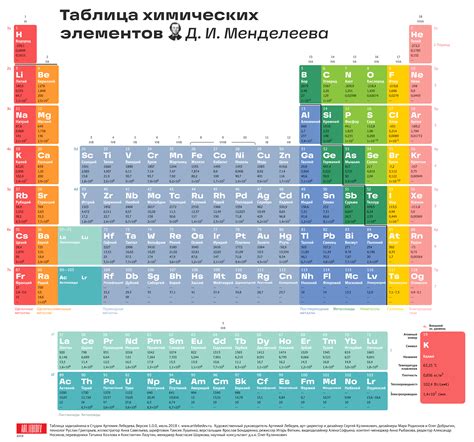
Химические элементы представляют собой вещества, которые не могут быть разложены на более простые с помощью химических методов. Каждый химический элемент обладает своими особенностями, которые определяют его взаимодействие с другими веществами.
Одна из особенностей химических элементов - их атомная структура. Каждый химический элемент имеет определенное количество протонов в атомном ядре, что определяет его атомный номер. Также у элемента может быть различное число нейтронов и электронов.
Основные химические элементы имеют свои символы, которые используются для их обозначения в химических формулах и уравнениях. Например, для обозначения кислорода используется символ O, а для углерода - C.
Химические элементы могут быть распределены по периодам и группам в таблице Менделеева. Периоды отображают количество энергетических уровней в атоме элемента, а группы - общее количество электронов на внешнем энергетическом уровне. Это позволяет классифицировать элементы и определить их свойства и взаимодействие с другими веществами.
Особенности химических элементов также определяют их физические и химические свойства, такие как температура плавления и кипения, электроотрицательность, химическая активность и способность образовывать соединения.
Некоторые элементы обладают особыми свойствами:
- Гелий (He) - самый легкий газ, не имеющий цвета, запаха и вкуса. Он обладает очень низкой плотностью и низкой температурой кипения, что делает его полезным в аэростатике и в жидрогенераторах.
- Кислород (O) - важный элемент для дыхания и горения. Он образует оксиды с различными элементами и присутствует в большом количестве в атмосфере Земли.
- Углерод (C) - ключевой элемент в органической химии. Он образует множество соединений, включая углеводороды, белки, жиры и глюкозу.
- Золото (Au) - благодаря своей красивой желтой окраске, золото было использовано для украшений и декоративных предметов с давних времен. Оно также обладает хорошей электропроводностью и устойчивостью к окислению.
Применение химии в повседневной жизни

Одно из наиболее распространенных применений химии - это производство пищевых продуктов. Химические реакции используются для сохранения продуктов, улучшения их вкуса и аппетитности, а также для создания разнообразных добавок, консервантов и красителей.
Химия также находит применение в сфере медицины. Благодаря химическим веществам и препаратам мы можем справиться с различными заболеваниями, болезнями и состояниями. Лекарственные препараты синтезируются с использованием химических реакций и компонентов, которые способны влиять на организм человека и вызывать определенные реакции.
Чистящие средства, которые мы используем в повседневной жизни, также содержат химические составляющие. Они помогают нам бороться с грязью, пылью и бактериями, обеспечивая нашему дому чистоту и гигиену.
В сфере развлечений и технологий также активно используется химия. Процессы окрашивания волос, создания косметических средств, производства аккумуляторов для электронных устройств - все это основано на химическом знании и применении соответствующих веществ.