Атом - это основная единица состава вещества. В физике атом определяется как наименьшая частица элемента, которая сохраняет его химические свойства. Атомы состоят из трех основных частиц - протонов, нейтронов и электронов.
Протоны имеют положительный заряд, нейтроны не имеют заряда, а электроны - отрицательный заряд. В зависимости от числа протонов в ядре атома их свойства изменяются. Например, водород состоит из одного протона и одного электрона, кислород имеет в своем ядре восемь протонов и восемь нейтронов.
Молекула - это группа атомов, связанных химическими связями. Молекулы образуются в результате химических реакций, где атомы обмениваются электронами, образуя стабильные соединения. Например, вода состоит из двух атомов водорода и одного атома кислорода, связанных вместе с помощью ковалентных связей.
Определение и структура атома
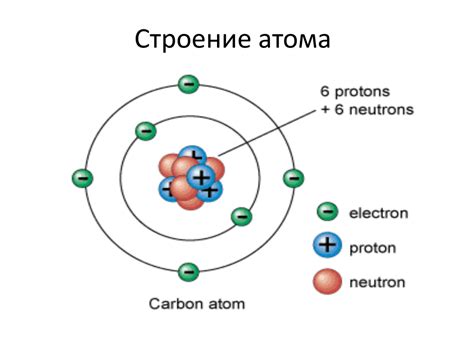
Протоны - это положительно заряженные частицы, которые находятся в ядре атома. Их количество определяет химические свойства элемента и называется атомным номером. Количество протонов также определяет электрический заряд атома.
Нейтроны - это нейтральные по заряду частицы, которые находятся в ядре атома. Они не имеют электрического заряда и их количество может меняться в разных атомах одного элемента.
Электроны - это отрицательно заряженные частицы, которые находятся вокруг ядра атома. Они движутся по определенным орбитам или энергетическим уровням. Количество электронов также определяет электрический заряд атома.
Структура атома можно представить в виде электронной оболочки, которая состоит из нескольких энергетических уровней, на которых находятся электроны. Ближайший к ядру уровень содержит меньшее количество электронов, чем более удаленные уровни.
Число протонов и электронов в атоме обычно совпадает, что делает его электрически нейтральным. Однако, при наличии различного количества электронов и протонов, атом может обладать положительным или отрицательным зарядом, что делает его ионом.
Таким образом, атомы с разным количеством протонов называются разными элементами, а их сочетания и взаимодействия образуют молекулы и различные химические соединения.
Свойства и взаимодействия атомов
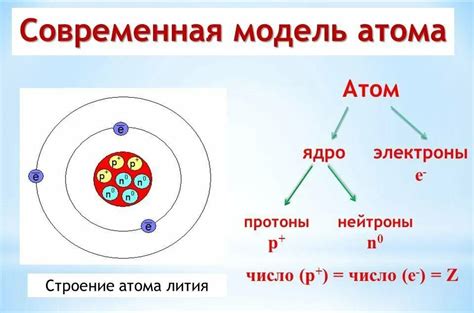
Протоны имеют положительный заряд, нейтроны не имеют заряда, а электроны имеют отрицательный заряд. Благодаря этим зарядам, атомы обладают электростатической притягивающей и отталкивающей силами. Протоны и электроны притягиваются друг к другу, в то время как протоны внутри ядра отталкиваются друг от друга из-за их одинакового заряда.
Электроны, находящиеся на разных энергетических уровнях, обладают разными свойствами. Нижние энергетические уровни могут вмещать меньшее количество электронов, чем высшие уровни. Каждый электрон имеет свой уникальный энергетический уровень, который определяет его поведение и способность взаимодействовать с другими атомами.
Атомы могут образовывать различные типы связей и соединений между собой. Одним из наиболее распространенных типов связей является ковалентная связь, при которой атомы обмениваются электронами. Другим типом связи является ионная связь, при которой один атом передает или получает электроны от другого атома. Водородная связь - это слабая связь, в которой атомы водорода притягиваются к электроотрицательным атомам.
Взаимодействия между атомами являются основой для образования молекул и различных химических соединений. Атомы могут объединяться в цепочки, кольца и трехмерные структуры, образуя сложные молекулы с уникальными свойствами.
| Пример | Тип связи |
|---|---|
| Молекула воды (H2O) | Ковалентная связь |
| Хлорид натрия (NaCl) | Ионная связь |
| ДНК (дезоксирибонуклеиновая кислота) | Сложная структура |
Молекула и ее состав
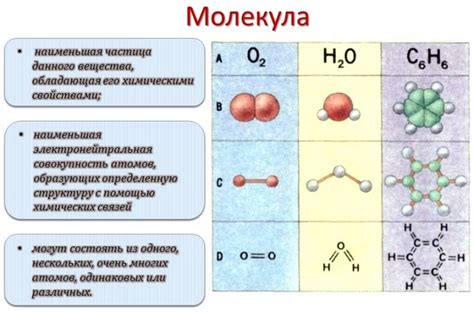
Молекулы могут быть составлены из одного типа атомов (например, кислородные молекулы, состоящие только из атомов кислорода) или различных типов атомов (например, вода, состоящая из атомов кислорода и водорода).
Состав молекулы определяется количеством и типами атомов, а также способом их соединения. Каждый атом в молекуле имеет свою роль и может выполнять определенные функции. Например, в молекуле воды один атом кислорода связан с двумя атомами водорода, и такая комбинация даёт молекуле уникальные свойства и способность образовывать водородные связи.
Молекулы могут образовывать различные структуры и формы, например, линейные, кольцевые или трехмерные. Их свойства, состояния и реактивность зависят от их состава и атомного строения.