Плавление вещества является одним из наиболее интересных и важных процессов в химии. В процессе плавления твердого вещества его молекулы переходят из упорядоченной решетки в некоторый более свободный состояния, где они могут перемещаться более свободно. Таким образом, плавление является фазовым переходом от твердого состояния к жидкому.
Молекулярные изменения, происходящие при плавлении вещества, связаны с разрушением межмолекулярных сил притяжения и переходом молекул в движение. В результате этого процесса происходят изменения внутренней энергии и структуры вещества.
В зависимости от химического состава и структуры вещества, а также условий плавления (температура, давление), молекулы могут переходить в жидкую фазу по-разному. Некоторые вещества могут иметь низкую температуру плавления, при которой их молекулы легко изменяют свою структуру и самих веществ можно сместить. Другие вещества, наоборот, имеют высокую температуру плавления, и их молекулы крайне устойчивы в своей структуре, что и создает высокие температуры.
Важно отметить, что плавление вещества является обратным процессом к затвердеванию. Это означает, что при охлаждении жидкого вещества его молекулы снова переходят в упорядоченное твердое состояние, что сопровождается выделением тепла.
Изменение структуры
При плавлении вещества происходят значительные изменения в структуре его молекул. В процессе плавления твердое вещество превращается в жидкое за счет разрушения и перегруппировки связей между атомами или ионами. Атомы или ионы начинают двигаться с большей свободой, и в результате молекулы располагаются в новом порядке.
Наиболее ярким примером изменения структуры при плавлении является твердое вещество, состоящее из кристаллической решетки. В решетке кристалла атомы или ионы упорядочены в определенном порядке и имеют строго определенное пространственное расположение.
Однако при плавлении кристаллическая решетка разрушается, и атомы или ионы начинают перемещаться в случайном порядке. В результате образуется жидкость, в которой частицы играют роль большого количества микроскопических шариков, свободно перемещающихся внутри друг друга.
Таким образом, плавление вещества влечет за собой значительные изменения в структуре его молекул, что обусловливает возможность изменения его агрегатного состояния.
Потеря кристалличности

При плавлении вещества происходят изменения молекул, в результате которых может произойти потеря кристалличной структуры. Кристалличность характеризуется упорядоченным расположением атомов или молекул вещества в решетке, что обеспечивает его специфические физические и химические свойства.
При повышении температуры вещество начинает плавиться, то есть переходит из твердого состояния в жидкое. В этот момент молекулы начинают терять свою кристалличность и перемещаются внутри жидкости в случайном порядке.
Потеря кристалличности влияет на свойства вещества. Например, при плавлении металлов, их кристаллическая решетка разрушается и образуется аморфная структура, которая имеет более плотную упаковку атомов. Это может привести к изменению механических свойств материала.
В некоторых случаях, при охлаждении жидкости обратно в твердое состояние, молекулы не успевают вернуться в исходную кристаллическую решетку, и вещество может образовать стеклообразную аморфную структуру.
Таким образом, плавление вещества сопровождается потерей кристалличности и может приводить к образованию новых фаз и изменению свойств материала.
Изменение энергии связи
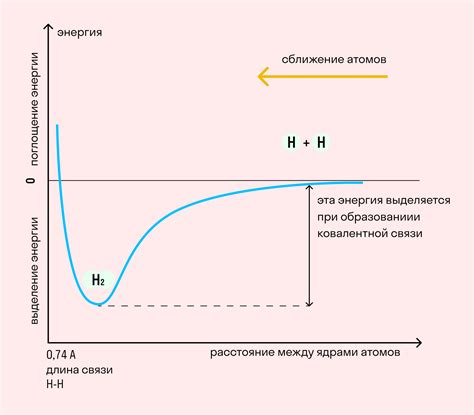
При плавлении вещества происходят значительные изменения в молекулах, в том числе в энергии связи.
Энергия связи - это энергия, необходимая для разрыва связи между атомами или молекулами. В процессе плавления, связи между атомами или молекулами ослабевают и становятся более подвижными, что приводит к изменению энергии связи.
Изменение энергии связи влияет на температуру плавления вещества. При повышении температуры, энергия связи уменьшается, и вещество начинает плавиться. При этом, энергия, которая ранее затрачивалась на поддержание связей между атомами или молекулами, преобразуется в кинетическую энергию и тепло.
На обратный процесс - затвердевание, влияет также изменение энергии связи. При охлаждении вещества, энергия связи увеличивается, связи становятся более прочными, что приводит к затвердеванию вещества. При этом, кинетическая энергия и тепло преобразуются обратно в энергию связи.
Изменение энергии связи при плавлении и затвердевании вещества играет важную роль в процессах перехода между фазами и определяет физические свойства вещества, такие как температура плавления, температура кипения и теплота плавления.
Фазовый переход
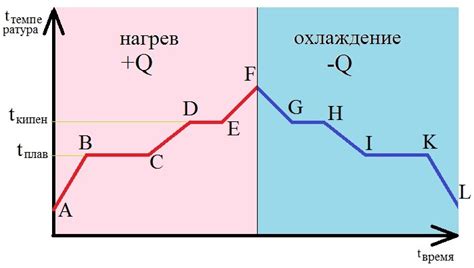
Плавление является одним из типичных примеров фазового перехода. В процессе плавления вещество переходит из твердого состояния в жидкое при достижении определенной температуры, называемой температурой плавления. В этот момент молекулы вещества начинают двигаться быстрее и распределяться не регулярным образом, что делает вещество твердым, а становятся перемешанными и плавными, что характерно для жидкости.
Фазовый переход сопровождается испусканием или поглощением тепла, в зависимости от того, происходит ли испарение или конденсация. При плавлении вещества тепло поглощается, так как молекулы вещества нужно "разорвать" связи, чтобы они могли двигаться свободно.
Фазовые переходы играют важную роль в природе и технологии. Изучение фазовых переходов позволяет понять, как вещества в различных фазах взаимодействуют друг с другом и какие процессы происходят на молекулярном уровне. Это помогает разрабатывать новые материалы и улучшать существующие технологии.
Изменение внутренней энергии
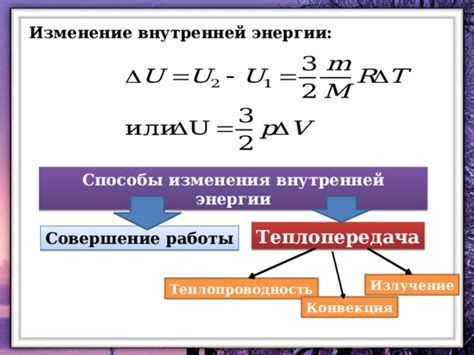
В процессе плавления, молекулы вещества получают энергию от окружающей среды в виде тепла. Это приводит к увеличению кинетической энергии молекул и расширению межмолекулярного расстояния. Когда температура достигает точки плавления, молекулы начинают свободно перемещаться, теряют упорядочение и становятся более подвижными.
В результате происходит изменение интра- и интермолекулярных связей. Интрамолекулярные связи ослабевают, а интермолекулярные связи разрушаются полностью или частично. Изменение внутренней энергии молекул приводит к изменению физических свойств вещества, таких как плотность, вязкость и теплоемкость.
Внутренняя энергия также связана с изменением фазового состояния вещества. Плавление является фазовым переходом с твердого состояния в жидкое. В этом процессе молекулы получают достаточно энергии, чтобы преодолеть силы притяжения и перейти в новую фазу.
| Фазовый переход | Изменение внутренней энергии |
|---|---|
| Твёрдое → жидкое | Увеличение |
| Жидкое → газообразное | Увеличение |
| Твёрдое → газообразное | Большое увеличение |
Влияние на физические свойства

Одним из основных физических свойств, которое изменяется при плавлении вещества, является температура плавления. Температура плавления вещества зависит от химического состава и молекулярной структуры вещества. При повышении температуры молекулы вещества начинают двигаться более активно, что приводит к разрушению связей между ними и переходу из твердого состояния в жидкое.
Также плавление вещества влияет на его плотность. При переходе из твердого состояния в жидкое вещество обычно расширяется и увеличивает свою объемную плотность. Однако, есть и исключения, например, лед, который при плавлении уменьшает свою плотность, что объясняет его плавание на поверхности воды.
Кроме того, плавление вещества может влиять на его вязкость. Вязкость – это мера сопротивления текучести вещества, и она может изменяться в зависимости от его состояния. Твердые вещества обычно обладают низкой вязкостью, а жидкости – более высокой. При плавлении вязкость вещества может уменьшаться, что делает его более текучим.
Таким образом, плавление вещества приводит к изменениям в его физических свойствах, таких как температура плавления, плотность и вязкость. Эти изменения связаны с молекулярной структурой вещества и определяют его поведение в различных условиях.
| Физическое свойство | Изменения при плавлении |
|---|---|
| Температура плавления | Повышение температуры приводит к разрушению связей между молекулами |
| Плотность | Обычно увеличивается, хотя есть исключения, например, лед |
| Вязкость | Уменьшается, делая вещество более текучим |