Атомы и ионы играют ключевую роль в химических реакциях. Хотя оба они являются фундаментальными частицами химических веществ, у них есть существенные отличия, которые сильно влияют на их поведение и взаимодействие.
Атомы представляют собой основные строительные блоки вещества. Они состоят из протонов, нейтронов и электронов. Протоны - положительно заряженные частицы, нейтроны - не несущие заряд частицы, а электроны - отрицательно заряженные частицы. В зависимости от количества протонов, определяется атомный номер, который определяет тип химического элемента. Атомы могут быть связаны друг с другом, образуя молекулы, или находиться в свободном состоянии.
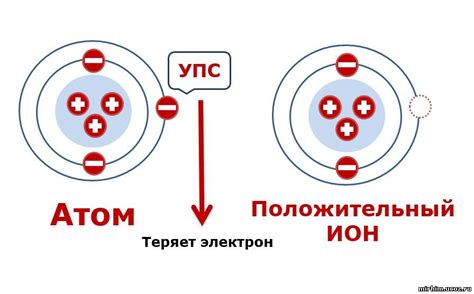
Ионы, в отличие от атомов, имеют различное количество электронов, что делает их заряженными. Когда атом теряет или приобретает электрон(ы), он становится положительно или отрицательно заряженным, и называется ионом. Ионы могут быть положительно заряженными (катионами), когда атом потерял один или несколько электронов, или отрицательно заряженными (анионами), когда атом приобрел один или несколько электронов. Эти заряженные частицы обладают различными химическими свойствами и могут сильно влиять на протекающие химические реакции.
Понятие атома и иона в химии
В химии явления и процессы вещественного мира изучаются с помощью понятий атома и иона.
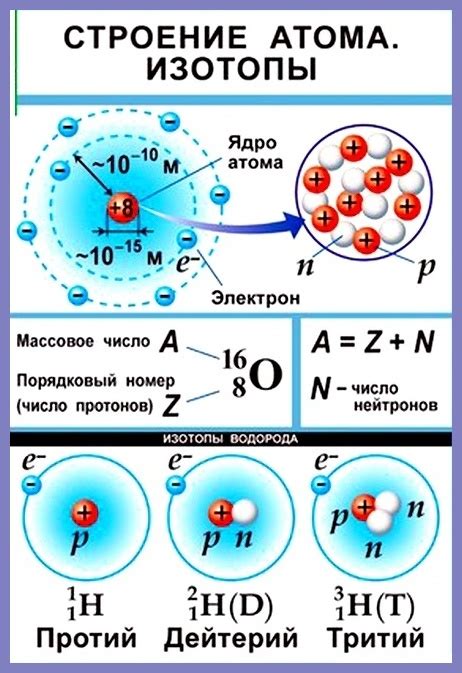
Атом – это наименьшая единица химического элемента, обладающая его свойствами. Атом состоит из протонов, нейтронов и электронов. Протоны и нейтроны находятся в ядре атома, а электроны вращаются по орбитам вокруг ядра. Количество протонов в атоме определяет его атомный номер и химические свойства, а сумма протонов и нейтронов – атомный массовый номер. Уникальные свойства каждого элемента определяются его атомным строением.
Ион – это атом или группа атомов, обладающая электрическим зарядом. Ионы образуются в результате взаимодействия атомов и молекул друг с другом. Ионы могут быть положительно или отрицательно заряженными, в зависимости от количества протонов и электронов в их составе. Положительно заряженные ионы называются катионами, а отрицательно заряженные – анионами. Ионы играют важную роль в химических реакциях, так как их взаимодействие позволяет образование новых веществ и изменение химических свойств вещества.
В итоге, понятие атома и иона – это основные строительные блоки химических реакций. Атомы образуют ионы, которые подвергаются различным превращениям и взаимодействиям, определяя при этом изменение состава и свойств вещества.
Определение атома

Атомы характеризуются своей атомной массой, которая указывается в таблице химических элементов. Атомная масса равна сумме масс протонов и нейтронов в атоме. Она измеряется в атомных единицах (а.е.м.) или Джонса (Da).
Атомы вещества могут быть одноатомными (например, атомы инертных газов), а также могут образовывать молекулы, состоящие из двух и более атомов одного или разных элементов.
| Элемент | Атомная масса (Da) |
|---|---|
| Водород | 1.00784 |
| Кислород | 15.999 |
| Углерод | 12.011 |
Определение иона

Катион – это положительно заряженный ион, образованный атомом, который потерял один или несколько электронов. Катионы имеют меньшее количество электронов по сравнению с количеством протонов в атоме.
Анион – это отрицательно заряженный ион, образованный атомом, который приобрел один или несколько электронов. Анионы имеют большее количество электронов по сравнению с количеством протонов в атоме.
Ионы играют важную роль в химических реакциях, образующих соединения. Заряд иона определяет его реактивность и способность к образованию соединений с другими ионами или нейтральными атомами.
Отличия атома от иона
Во время химических реакций атомы и ионы проявляют различные свойства и взаимодействуют с другими веществами по-разному. Вот некоторые основные отличия между атомами и ионами в химических реакциях:
1. Заряд: Атомы имеют нейтральный заряд, то есть количество протонов и электронов в атоме одинаково. Ионы же имеют заряд, отличный от нуля, так как количество протонов и электронов в ионе не совпадает.
2. Валентность: У атомов и ионов может быть разная валентность, то есть способность участвовать в химических связях. Атомы обычно обладают постоянной валентностью, в то время как ионы могут иметь различную валентность, в зависимости от количества потерянных или полученных электронов.
3. Взаимодействие: Атомы в химических реакциях обычно образуют химические связи с другими атомами, чтобы достигнуть электронной устойчивости. Ионы же взаимодействуют с другими ионами или атомами, образуя ионные связи или ковалентные связи.
4. Роль в реакциях: Атомы могут быть исходными веществами или продуктами в химических реакциях. Ионы же чаще всего участвуют в реакциях как исходные вещества или продукты, так как их заряд влияет на их активность и взаимодействие с другими веществами.
Таким образом, атомы и ионы имеют существенные различия, когда речь идет о их роли в химических реакциях.
Различия в электрическом заряде
Атомы являются электрически нейтральными частицами, так как количество протонов и электронов в них одинаково. Протоны имеют положительный заряд, а электроны – отрицательный. Поэтому суммарный электрический заряд атома равен нулю.
Ионы, в отличие от атомов, имеют отличное от нуля значение электрического заряда. Ионы образуются путем потери или приобретения электронов атомом. Если атом отдает электрон, то он становится положительно заряженным ионом, называемым катионом. Если атом принимает дополнительный электрон, то он становится отрицательно заряженным ионом, называемым анионом.
Различие в электрическом заряде между атомами и ионами является одним из факторов, определяющих их реакционную способность.
Различия в участии в химических реакциях

Атомы и ионы взаимодействуют друг с другом в химических реакциях, но у них есть определенные различия в том, как они принимают участие в этих реакциях.
1. Заряд: Главное различие между атомами и ионами состоит в их электрическом заряде. Атомы обычно имеют нейтральный заряд, так как число протонов в их ядре равно числу электронов в их облаке. В то время как ионы могут иметь положительный или отрицательный заряд из-за потери или получения электронов.
2. Реакционное участие: Атомы и ионы участвуют в химических реакциях, но ионы могут проявлять большую активность и, следовательно, большую склонность к реакциям. Ионы с положительным зарядом, называемые катионами, имеют тенденцию привлекать электроны и участвовать в реакциях с атомами или ионами с отрицательным зарядом, называемыми анионами.
3. Стабильность: Атомы стремятся образовывать молекулы или соединения, где их энергия наименьшая, и они имеют полные энергетические уровни. Ионы, с другой стороны, стремятся нейтрализовать свой заряд и стать энергетически более стабильными путем образования связей с другими ионами или атомами.
4. Реакционная способность: Ионы могут проявлять большую реакционную способность по сравнению с атомами. Это происходит из-за их различного электрического заряда и возможности образования электростатических взаимодействий с другими заряженными частицами.
5. Роль в электролитах: Ионы играют важную роль в электролитах, так как они могут двигаться под влиянием электрического поля, что позволяет возникнуть электрическому току. Атомы не могут так свободно двигаться, так как они не имеют зарядов, способных взаимодействовать с электрическим полем.
Итак, различия в участии атомов и ионов в химических реакциях можно объяснить их различными зарядами, реакционной способностью и ролями в электролитах, что делает ионы более активными и более склонными к реакциям, чем атомы.